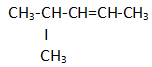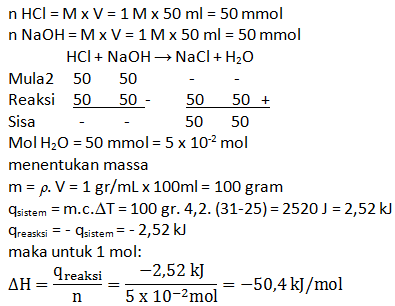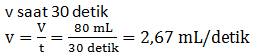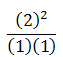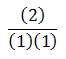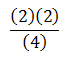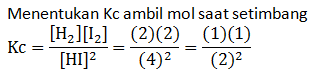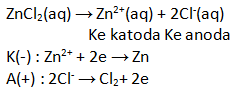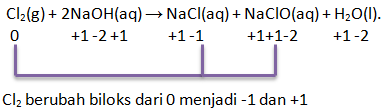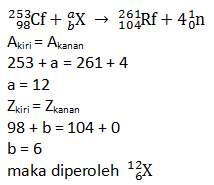DAFTAR ISI
Pembahasan Soal Ujian Nasional (UN) SMA Kimia 2015
Z:[Ne] 3s2 3p5
Apabila X dan Z bersenyawa, rumus senyawa yang terbentuk adalah
- X3Z
- X3Z2
- X2Z
- X2Z3
- XZ3
(bisa melepas 3e) membentuk X3+
Z:[Ne] 3s2 3p5 (menangkap 1 e) membentuk Z–
Jika keduanya berikatan maka akan melakukan ikatan ion (terjadi antara yang melepaskan e (ion +) dengan yang menangkap e (ion -) membentu senyawa XZ2 atau XZ3. Mekanismenya seperti berikut:
- X2+ + Z– (muatan X (2) menjadi jumlah atom Z, muatan Z (1) menjadi jumlah atom Z, sehingga menjadi XZ2)
- X3+ + Z– (muatan X (3) menjadi jumlah atom Z, muatan Z (1) menjadi jumlah atom Z, sehingga menjadi XZ3)
JAWABAN E
DOWNLOAD SOAL UN KIMIA 2015 DALAM BENTUK PDF KLIK DISINI
PEMBAHASAN :
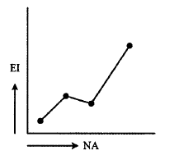
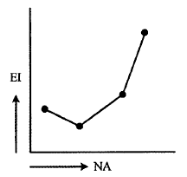
Di periode ketiga terdapat penyimpangan energi ionisasi (idealnya semakin besar nomor atom semakin besar energi ionisasi). Penyimpangan ini berupa naiknya energi ionisasi Mg, Hal ini dijelaskan dari konfigurasinya

Konfigurasi elektron yang penuh lebih stabil sehingga sulit untuk melepaskan elektron sehingga diperlukan energi yang besar artinya Energi ionisasi Mg lebih tinggi dibanding Al. Sehingga grafiknya:
LIHAT JUGA : Try Out Online UN
- Zat M : Senyawa kovalen non polar, Zat N : Senyawa Ionik
- Zat M : Senyawa kovalen non polar, Zat N : Senyawa kovalen polar
- Zat M : Senyawa kovalen non polar, Zat N : Logam
- Zat M : Senyawa kovalen polar, Zat N : Logam
- Zat M : Senyawa kovalen polar, Zat N : Senyawa Ionik
PEMBAHASAN :
Perbedaan senyawa ion, kovalen polar dan non polar di jelaskan tabel berikut
Maka dari data tabel M merupakan senyawa non polar karena titik leleh rendah dan tidak larut dalam air. Sedangkan N merupakan senyawa ionik karena larut dalam air dan lelehannya dapat menghantar listrik
JAWABAN A
LIHAT JUGA : Video Pembahasan UN Kimia 2014
- n = 3; l=0; m = -1; s = + ½
- n = 3; l=0; m = +1; s = – ½
- n = 3; l=1; m = +1; s = + ½
- n = 3; l=2; m = 0; s = – ½
- n = 3; l=1; m = 0; s = – ½
LIHAT JUGA : Video Pembahasan UN Kimia 2015
- Zn(s) + HCl(aq) → ZnCl(aq) + H(g)
- Zn(s) + HCl(aq) → ZnCl2(aq) + H2(g)
- Zn(s) + 2HCl(aq) → ZnCl2(aq) + H(g)
- Zn(s) + 2HCl(aq) → ZnCl2(aq) + H2(g)
- Zn(s) + 2HCl(aq) → ZnCl(aq) + H2(g)
PEMBAHASAN :
Logam seng : Zn(s)
Larutan asam klorida : HCl (aq)
Larutan seng klorida : Zn2+ + Cl– → ZnCl2 (aq)
Gas hidrogen : H2 (g), maka reaksinya
Zn(s) + 2HCl(aq) → ZnCl2(aq) + H2(g) (setelah disetarakan)
JAWABAN D
Suatu senyawa karbon terdiri dari 40% massa C, 6,7% massa H dan sisanya oksigen. Rumus molekul senyawa tersebut (Ar: C =12, H = 1, dan O =16) dan Mr senyawa 60 adalah….
- CH2O
- C2H4O2
- C2H2O
- C2H4O
- C2H4O4
- 4 : 3
- 3 : 4
- 3 : 2
- 2 : 3
- 2 : 1
PEMBAHASAN :
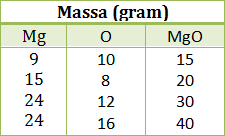
Untuk menentukan perbandingan massa Mg dan O dengan cara mudah yaitu dengan menjumlahkan massa Mg dan O dan jumlahnya tersebut harus sama dengan massa MgO. Untuk percobaan 4, penjumlahan massa Mg dan O sama dengan massa MgO, maka perbandingannya bisa ditentukan dari perbandingan massa Mg dan massa O
(Perc 4) Massa Mg : Massa O = 24 : 16 = 3: 2
JAWABAN C
- (1) dan (2)
- (2) dan (3)
- (3) dan (4)
- (4) dan (5)
- (5) dan (2)
PEMBAHASAN :
(1) proses pembersihan darah dalam ginjal merupakan contoh dari dialisis yaitu penyaringan ion-ion pengganggu melalui selaput semipermeabel
(2) pembentukan delta di muara sungai merupakan contoh dari koagulasi yaitu proses penggumpalan dari sistem koloid karena adanya ion lain yang berbeda muatan
(3) pembuatan ban kendaraan dari karet alam merupakan contoh dari koagulasi yaitu proses penggumpalan dari sistem koloid karena adanya ion lain yang berbeda muatan
(4) pembentukan karang oleh binatang merupakan contoh dari koagulasi yaitu proses penggumpalan dari sistem koloid karena adanya ion lain yang berbeda muatan.
JAWABAN A
- (1) dan (2)
- (1) dan (3)
- (2) dan (3)
- (2) dan (5)
- (3) dan (4)
PEMBAHASAN :
(1) desalinasi air laut merupakan proses reversible osmosis,berkaitan dengan sifat koligatif tekanan osmosis yaitu tekanan yang diperlukan untuk menghentikan proses osmosis
(2) penggunaan etilen glikol pada radiator mobil merupakan penerapan penurunan titik beku. Etilen glikol ditambahkan agar menurunkan titik beku air
(3) cairan infus yang dimasukkan ke dalam darah berkaitan dengan proses osmosis
(4) proses merambatnya air pada akar tanaman berkaitan dengan proses osmosis
(5) penggunaan garam pada pembuatan es puter berfungsi untuk menurunkan titik beku air untuk mendinginkan es puter
JAWABAN D
- 0,074 gram
- 0,148 gram
- 0,232 gram
- 0,288 gram
- 0,370 gram
PEMBAHASAN :
Gunakan rumus titrasi
a. Ma. Va = b. Mb. Vb
1.0,1M. 20 = 2. nbasa
n = 1 mmol
Gr = n x Mr = 1 x 74 = 74 mgram = 0,074 gram
JAWABAN A
Senyawa/ion yang berfungsi sebagai penyangga pada cairan luar sel adalah….
- (1) dan (2)
- (1) dan (3)
- (2) dan (3)
- (3) dan (4)
- (4) dan (5)
PEMBAHASAN :
Senyawa/ion yang berfungsi sebagai penyangga pada cairan luar sel adalah H2CO3 dan HCO3– sedangkan senyawa/ion yang berfungsi sebagai penyangga intra/di dalam sel adalah H2PO4– dan HPO42-
JAWABAN E
- 1- log8
- 1-1og 4
- 1-log 2
- 13 + log 2
- 13 + log 8
- 6 gram
- 9 gram
- 60 gram
- 100 gram
- 120 gram
- 1 – log 5
- 1 + log 5
- 5 + log 1
- 9 + log 1
- 9 + log 5
- (1) dan (2)
- (1) dan (3)
- (2) dan (3)
- (2) dan(4)
- (3) dan (4)
PEMBAHASAN :
Elektrolit Kuat terdiri dari asam kuat, basa kuat dan garam
Elektrolit lemah terdiri dari asam lemah, basa lemah
Non elektrolit : Glukosa, urea , alkohol
- HNO3 (asam kuat) : elektrolit kuat
- H2SO4 (asam kuat) : elektrolit kuat
- NH4OH (basa lemah) : elektrolit lemah
- C6H12O6 : non elektrolit
JAWABAN A
Suatu bahan makanan diuji dengan :
- pereaksi biuret terbentuk warna ungu
- pereaksi timbal (II) asetat terbentuk warna hitam
Berdasarkan hasil uji tersebut dapat disimpulkan dapat disimpulkan bahwa bahan makanan tersebut mengandung….
- Zat : Protein, Jenis Kandungan : Sistein
- Zat : Protein, Jenis Kandungan : Tirosin
- Zat : Karbohidrat, Jenis Kandungan : Amilum
- Zat : Protein, Jenis Kandungan : Glisin
- Zat : Karbohidrat, Jenis Kandungan : Glukosa
PEMBAHASAN :
Pereaksi biuret akan membentuk warna ungu jika dimasukkan ke dalam zat yang mengandung protein. Sedangkan, peraksi timbal akan membentuk warna hitam jika dimasukan ke dalam asam amino yang mengandung unsur belerang (s). Asam amino yang mengandung unsur belerang yaitu sistein
JAWABAN A
- (1) dan (2)
- (1) dan (3)
- (2) dan (3)
- (3) dan (4)
- (4) dan (5)
PEMBAHASAN :
(1) biokatalis atau enzim merupakan fungsi dari protein
(2) mengatur metabolisme lemak merupakan fungsi dari karbohidrat
(3) membentuk struktur sel jaringan merupakan fungsi dari karbohidrat
(4) memperbaiki sel yang rusak merupakan fungsi dari protein
(5) cadangan energi merupakan fungsi dari protein dan lemak.
Fungsi lain dari karbohidrat:
- Sumber energi utama bagi tubuh
- Menjaga keseimbangan asam-basa tubuh
- Membantu penyerapan kalsium
- Melancarkan pencernaan
JAWABAN C
- (1) dan (2)
- (1) dan (3)
- (2) dan (3)
- (3) dan (4)
- (4) dan (5)
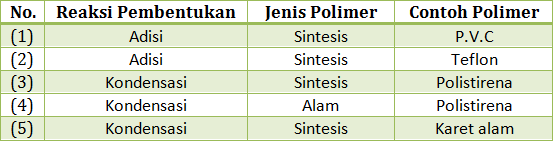
PEMBAHASAN :
- P.V.C merupakan polimer sintesis yang dibentuk melalui reaksi adisi
- Teflon merupakan polimer sintesis yang dibentuk melalui reaksi adisi
- Polisirena merupakan polimer sintesis yang dibentuk melalui reaksi adisi
- Karet alam merupakan polimer alam yang dibentuk melalui reaksi adisi
JAWABAN A
- (1) dan (2)
- (1) dan (3)
- (2) dan (3)
- (2) dan (4)
- (3) dan (5)
PEMBAHASAN :
- Kloro etana : pembuatan tetraetil timbal yang ditambahkan ke dalam bensin untuk memperbaiki bilangan oktan
- Asam formiat : digunakan sebagai bahan koagulan untuk meng-koagulasi karet dari lateks
- Iodoform : Antiseptik
- Monosodium glutamat : penyedap rasa
- Glikol : Anti beku pada air radiator
JAWABAN E
- 2 metil, butana
- 3 – metil, 2 – pentena
- 2 – metil, 3 – pentena
- metil siklo pentana
- 2 – metil pentana
PEMBAHASAN :
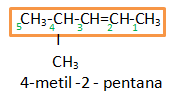
JAWABAN Tidak Ada Pilihan
Suatu senyawa memiliki rumus molekul C4H8O. Jika bereaksi dengan larutan Tollens menghasilkan endapan perak. Senyawa tersebut adalah….
- butanal
- butanol
- butanon
- 2-metil pentanal
- 2-metil propanon
PEMBAHASAN :
C4H8O kemungkinan aldehid atau keton. Untuk membedakan aldehid dan keton salah satunya direaksikan dengan pereaksi tollens. Aldehid akan membentuk endapan cermin perak jika bereaksi dengan tollens sedangkan keton tidak bereaksi, karena C nya ada 4 maka jawabannya yaitu butanal.
JAWABAN A
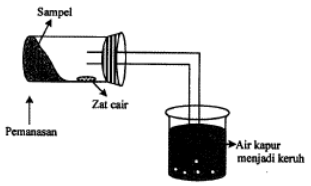
Berubahnya air kapur menjadi keruh membuktikan adanya
- hidrogen dan oksigen
- karbon dan oksigen
- oksigen dan nitrogen
- nitrogen dan kobalt
- kalsium dan oksigen
PEMBAHASAN :
Berubahnya air kapur menjadi keruh, akibat adanya gas CO2 yang bereaksi dengan air kapu Ca(OH)2 membentuk endapan CaCO3 sehingga menjadi keruh
CO2(g) + Ca(OH)2(aq) → CaCO3(s)
Maka zat yang menyebabkan keruh air kapur yaitu CO2 yang terdiri dari unsur C dan O
JAWABAN B
Nama senyawa tersebut adalah….
- meta-kloro fenol
- orto-kloro fenol
- 4-kloro fenol
- hidroksi benzena klorida
- hidroksi kloro benzena
PEMBAHASAN :
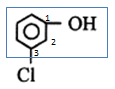
posisi 1,3 yaitu meta. Kloro menjadi cabang karena prioritas lebih rendah, sehingga namanya menjadi meta kloro fenol
JAWABAN A
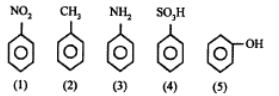
Senyawa yang digunakan sebagai pelarut dan desinfektan berturut-turut adalah..
- (1) dan (2)
- (2) dan (3)
- (2) dan (5)
- (3) dan (4)
- (4) dan (5)
PEMBAHASAN :
- Nitrobenzen berfungsi sebagai bahan peledak, pembuatan anilin, dan parfum pada sabun.
- Toluena memiliki kegunaan sebagai bahan dasar pembuatan asam benzoat, bahan peledak TNT, dan sebagai pelarut
- Anilin memiliki kegunaan pembuatan zat warna diazo, obat-obatan, bahan bakar roket dan bahan peledak.
- Benzensulfonat memiliki kegunaan sebagai pemanis buatan
- Fenol sebagai desinfektan dalam karbol
JAWABAN C
- -218,00 kJ
- -235,50 kJ
- -276,60 kJ
- -335,20 kJ
- -344,60 kJ
PEMBAHASAN :
Jalan I (langsung) = Jalan II (tidak langsung)
∆H1 = ∆H2 + ∆H3
∆H1 = -276,6 + (-58,6) = -335,2 kJ
JAWABAN D
- -25,20 kJ
- -50,40 kJ
- -54,60 kJ
- -55,44 kJ
- -57,10 kJ
- (1) dan (2)
- (1) dan (3)
- (2) dan (3)
- (2) dan (4)
- (3) dan (4)
PEMBAHASAN :
Contoh reaksi endoterm
- Fotosintesis tumbuhan
- Menjemur pakaian
- Cracking alkana
- Reaksi dekomposisi termal
- Es batu mencair
Contoh reaksi eksoterm
- Respirasi
- Polimerisasi
- Reaksi korosi
- Reaksi netralisasi
- Reaksi pembakaran
JAWABAN D
Pada percobaan reaksi antara logam aluminium dan asam sulfat sesuai persamaan reaksi:2 Al (s) + 3 H2SO4 (aq) → Al2(SO4)3 (aq) + 3H2 (g)
Gas hidrogen ditampung dan diukur volumenya pada temperatur yang tetap. Data pengukuran tiap waktu sesuai tabel berikut:
Laju reaksi pembentukan gas hidrogen setelah 30 detik sebesar
- 0,83 mL/detik
- 1,33 mL/detik
- 2,67 mL/detik
- 2,50 mL/detik
- 7,50 mL/detik
2HCl(g) ↔ H2(g) + Cl2(g)
Jika pada keadaan tersebut diperoleh data :

Perubahan Iaju reaksi yang terjadi pada percobaan (1) dan (3) dipengaruhi oleh….
- konsentrasi
- suhu
- luas permukaan
- katalis
- waktu
PEMBAHASAN :
Percobaan 1 dan 3 memiliki waktu reaksi yang berbeda hal tersebut disebabkan karena perbedan suhu (lihat yang bedanya antara percobaan 1 dan 3)
JAWABAN B
- kanan karena nilai K semakin besar
- kiri karena nilai K semakin kecil
- kanan karena nilai K semakin kecil
- kiri karena nilai K tetap
- kanan karena nilai K tetap
PEMBAHASAN :
Nilai K bergantung pada suhu, jika suhu tetap maka nilai K tidak berubah.Jika konsentrasi salah satu zat ditambah maka reaksi akan bergeser menjauhi zat yang ditambah. Karena yang ditambah amoniak (NH3) yang berada di sebelah kiri maka reaksi akan bergeser ke kanan
JAWABAN E
- 7,94 gram
- 15,88 gram
- 23,82 gram
- 31,75 gram
- 39,69 gram
- 2H2O(l) → 4H+(aq) + O2(g) + 4e
- 4OH–(aq) → 2H2O(l) + O2 + 4e
- C(s) + O2 (g) → CO2(g)
- 2Cl–(aq) → Cl2(g) + 2e
- Zn2+(aq) → Zn(s) + 2e
- Cl2, dari -1 menjadi + 1 dan 0
- Cl2, dari +1 menjadi -1 dan 0
- NaOH, dari 0 menjadi -1 dan +1
- NaOH, dari -1 menjadi+1 dan 0
- Cl2, dari 0 menjadi -1 dan +1

Paku yang mengalami perkaratan paling lambat adalah ….
- (1)
- (2)
- (3)
- (4)
- (5)
PEMBAHASAN :
Pengkaratan disebabkan karena ada faktor udara (O2) dan air (H2O). Agar pengkaratan lebih lambat maka harus ditempatkan dalam wadah yang mengurangi bersentuhan dengan air dan udara.
- Wadah terbuka berarti bersentuhan dengan udara
- Wadah terbuka tetapi disimpan zat penarik air
- Ditempat dalam air akan terjadi korosi
- Ditempatkan dalam wadah berisi minyak, paku akan paling lambat berkarat karena tidak bersentuhan dengan air dan udara
- Ditempatkan dalam wadah berisi larutan garam akan mempercepat terjadinya pengkaratan
JAWABAN D
Cu2+(aq) + 2e → Cu(s) Eo = +0,34 V
Al3+(aq) + 3e → Al(s) Eo = -1,70 V
Zn2+(aq) + 2e → Zn(s) Eo = -0,76 V
Ag+(aq) + 1e → Ag(s) Eo = +0,80 V
Fe2+(aq) + 2e → Fe(s) Eo = -0,44 V
- Ag/Ag+ // Cu2+/Cu
- Cu/Cu2+//Al3+/Al
- Cu/Cu2+ // Ag+/Ag
- Fe/Fe2+ // Zn2+/Zn
- Fe/Fe2+ // Al3+/Al
PEMBAHASAN :
Berlangsung spontan jika Eo sel bernilai positif
Eosel = Eokatoda – Eoanoda
Dalam notasi sel anoda berada di sebelah kiri dan katoda berada di sebelah kanan
- Eosel = EoCu – EoAg = +0,34 – 0,80 = -0,46 volt
- Eosel = EoAl – EoCu = -1,70 – 0,34 = -2,04 volt
- Eosel = EoAg – EoCu = +0,80 – 0,34 = +0,46 volt
- Eosel = EoZn – EoFe = -0,76 – (-0,44) = -0,32 volt
- E. Eosel = EoAl – EoFe = -1,70 – (-0,44) = -1,26 volt
JAWABAN C
Nuklida X pada persamaan reaksi inti tersebut adalah ….
- (1) dan (2)
- (1) dan (3)
- (2) dan (3)
- (2) dan (4)
- (3) dan (4)
PEMBAHASAN :
Kriolit : Na3AlF6
Posforit : Ca3(PO4)2
Pyrolusit : MnO2
Asbes : Mg3(Si205)(OH)4
JAWABAN B
(1) makin besar nomor atomnya makin kuat sifat asamnya
(2) terdiri dari unsur logam, non logam dan metaloid
(3) makin besar nomor atom makin banyak elektron valensinya
(4) makin besar nomor atom makin kuat sifat oksidatornya
Sifat-sifat tersebut dimiliki oleh unsur…
- periode 1
- periode 3
- periode 4
- golongan halogen
- golongan gas mulia
PEMBAHASAN :
(1) Makin ke kanan sifat asam makin kuat berarti bukan satu golongan tapi satu periode
(2) terdiri dari unsur logam (Na,Mg, Al), non logam(P, S, Cl) dan metaloid (Si) : Periode ketiga
(3) makin besar elektron valensi menunjukan golongan, yaitu dari kiri ke kanan dari IA sampai VIII A
(4) makin ke kanan sifat oksidator makin besar
Jadi jawabnnya periode ketiga
JAWABAN B
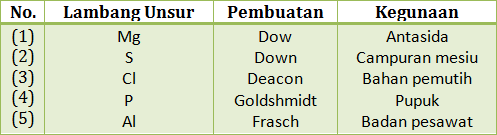
- 1 dan 2
- 1 dan 3
- 2 dan 3
- 2 dan 4
- 4 dan 5
PEMBAHASAN :
- Mg, pembuatan Down, kegunaaan antasida
- S, pembuatan Frasch & sisilia, kegunaan pembuatan asam sulfat, vulkanisasi karet, obat penyakit kulit, dan membasmi penyakit tanaman
- Cl, pembuatan Deacon dan Weldon, kegunaan kaporit, pemutih
- P, pembuatan Wohler, kegunaan pembuatan korek api, pelapis logam, pupuk.
- Al, pembuatan Hall-Heroult, kegunaan rangka baja, bahan alat masak.
JAWABAN B
DOWNLOAD SOAL UN KIMIA 2015 DALAM BENTUK PDF KLIK DISINI