Contoh Soal & Pembahasan Hidrolisis
PEMBAHASAN :
Reaksi antara ion garam dengan air.
PEMBAHASAN :
Hidrolisis parsial yaitu bereaksinya sebagian ion dari garam dengan air. Contohnya pada garam yang terbentuk dari Asam lemah dan basa kuat CH3COONa. Yang bereaksi dengan air hanya ion CH3COO–, ion Na+ tidak bereaksi dengan air
PEMBAHASAN :
Tidak semua garam dapat mengalami hidrolisis. Beberapa jenis garam diantaranya:
- Garam dari asam kuat dan basa kuat, contoh : NaCl tidak mengalami hidrolisis
- Garam dari asam lemah dan basa kuat atau dari asam kuat dan basa lemah mengalami hidrolisis parsial/sebagian, contohnya: KCN atau AgCl
- Garam dari asam lemah dan basa lemah, mengalami hidrolisis sempurna/total, contohnya : CH3COOCN
a. Pb(NO3)2
b. (NH4)2CO3
c. KNO3
d. MgSO4
e. Na2HPO4
Na+ + H2O → tidak bereaksi HPO42- + H2O → H2PO4– + OH– (terhidrolisis sebagian/parsial)
- AlCl3
- CuSO4
- Ba(NO3)2
- KCN
- Na2CO3
PEMBAHASAN :
Untuk menentukan sifat asam atau basa suatu garam, bisa menentukan langsung dari asam atau basa penyusunnya. Sifat garam akan mengikuti asal yang bersifat kuat. Jika yang kuat asam maka garam akan bersifat asam, jika yang kuat basa maka yang garam bersifat basa. Jika keduanya kuat akan bersifat netral. Jika keduanya lemah, maka akan bergantung pada nilai Ka dan Kb
- AlCl3 bersifat asam karena berasal dari asam kuat HCl dan basa lemah Al(OH)3, jika dimasukan lakmus merah akan berwarna merah. Jika dimasukan lakmus biru akan berwarna merah
- CuSO4 bersifat asam karena berasal dari asam kuat H2SO4 dan basa lemah Cu(OH)2, jika dimasukan lakmus merah akan berwarna merah. Jika dimasukan lakmus biru akan berwarna merah
- Ba(NO3)2 bersifat netral karena berasal dari asam kuat HNO3 dan basa kuat Ba (OH)2, jika dimasukan lakmus merah akan berwarna merah. Jika dimasukan lakmus biru akan berwarna biru
- KCN bersifat basa karena berasal dari asam lemah HCN dan basa kuat KOH, jika dimasukan lakmus merah akan berwarna biru. Jika dimasukan lakmus biru akan berwarna biru
- Na2CO3 bersifat basa karena berasal dari asam lemah H2CO3 dan basa kuat NaOH, jika dimasukan lakmus merah akan berwarna biru. Jika dimasukan lakmus biru akan berwarna biru
- CH3COONa 1 M (Ka CH3COOH = 1 x 10-5)
- NH4Cl 0,1 M (Kb NH4OH = 1 x 10-5)

Soal No.7
Larutan CH3COOH 0,15 M yang volumenya 100 mL dicampur dengan 150 mL larutan NaOH 0,1 M (Ka CH3COOH = 10-5). Berapakah pH campuran tersebut?
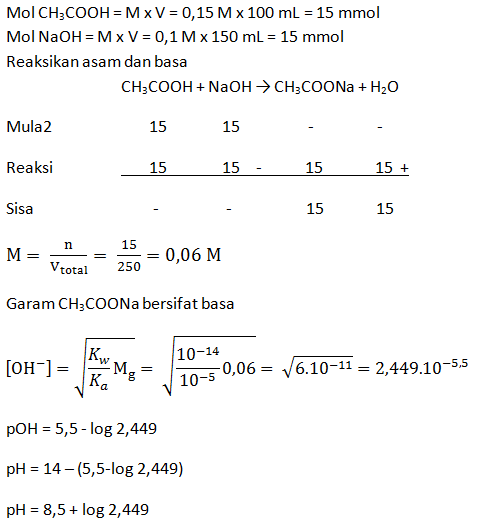
PEMBAHASAN :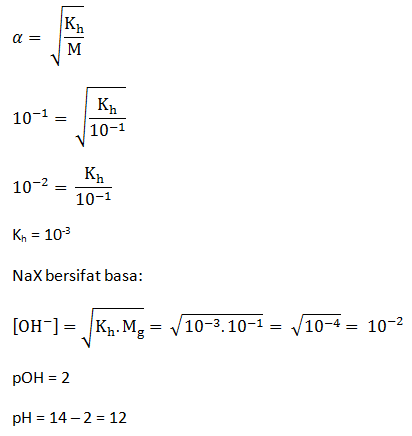
- Larutan NaCN 0,1 M (Ka HCN = 4 x 10-6)
- CH3COONH4 0,1 M ( Ka CH3COOH = 1 x 10-5 dan Kb NH3 = 1 x 10-5)
- Campuran 100 mL CH3COOH 0,1 M dengan 100 mL larutan NaOH 0,1 M (Ka = 1 x 10-5)
- Campuran 200 mL NH3 0,3 M dengan 300 mL HCl 0,2 M (Kb = 1 x 10-5)
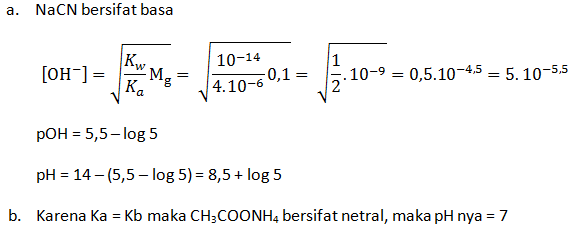
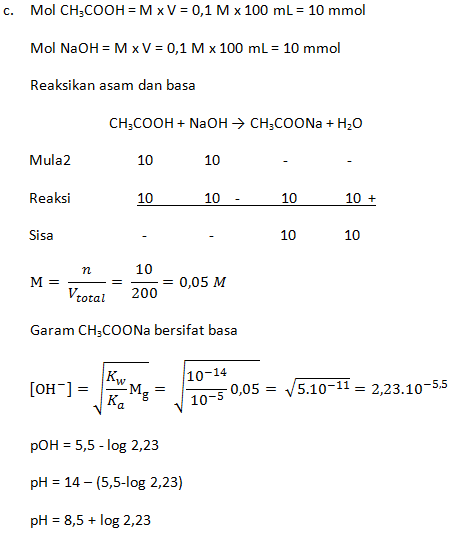
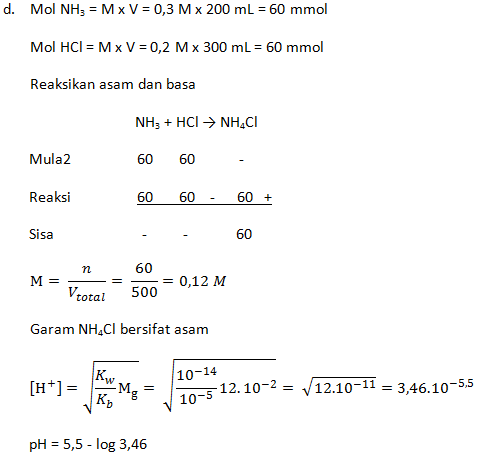
PEMBAHASAN :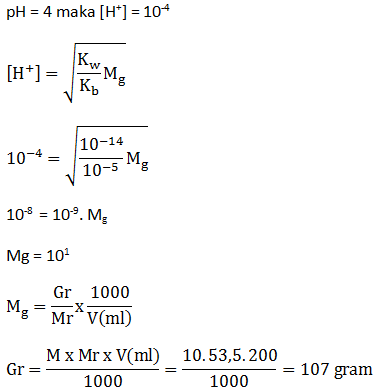
Sumber Soal : KIMIA Kelas XI Pengarang Unggul Sudarmo, Penerbit Erlangga

mau tanya soal nomor 10.
pH = 4 kan berarti [H+] = 10^-4
berarti kalau ada soal pH = 6, [H+] = 10^-6 ya?
betul