Kumpulan Soal Ulangan Laju Reaksi Dengan Pembahasannya
- berkurangnya konsentrasi A per satuan waktu
- berkurangnya konsetrasi C per satuan waktu
- bertambahnya konsentrasi B per satuan waktu
- bertambahnya konsentrasi A dan B per satuan waktu
- berkurangnya konsetrasi C dan D per satuan waktu
PEMBAHASAN :
Laju reaksi merupakan berkurangnya konsentrasi pereaksi per satuan waktu atau bertambahnya konsentrasi produk per satuan waktu. A dan B merupakan pereaksi sedangkan C dan D merupakan produk. Sehingga ungkapan yang tepat adalah berkurangnya konsentrasi A atau B per satuan waktu atau bertambahnya konsentrasi C dan D per satuan waktu. Sehingga jawaban yang paling tepat adalah A
Jawaban A
DOWNLOAD KUMPULAN SOAL ULANGAN LAJU REAKSI DALAM BENTUK PDF KLIK DISINI
- 10-2 M det-1
- 3 x 10-2 M det-1
- 3 x 1-3 M det-1
- 4 x 10-3 M det-1
- 10-3 M det-1
PEMBAHASAN :
Menentukan laju fosgen dapat ditentukan dari rumus:
![]()
![]()
Jawaban C
2NO(g) +2H2(g) → N2(g) + 2H2O(g)
diperoleh data percobaan sebaga berikut :
- V = k[NO][H2]
- V = k[NO]2[H2]
- V = k[NO]
- v = k[NO][H2]2
- v =k[H2]
PEMBAHASAN :
Menentukan persamaan laju reaksi harus menentukan orde reaksinya terlebih dahulu
Menentukan orde NO : cari 2 [H2] yang sama (percobaan 1 dan 2)
![]()
![]()
![]()
x = 1
Menentukan orde H2 : cari 2 [NO] yang sama (percobaan 2 dan 4)
![]()
![]()
![]()
y = 1
maka persamaan laju reaksinya adalah v = k[NO][H2]
Jawaban A
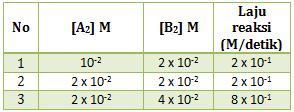
Perhatikan data percobaan dari reaksi berikut :
- 5 x 102
- 5 x 10-3
- 5 x 104
- 1,25 x 10-2
- 1,25 x 102
PEMBAHASAN :
Untuk menentukan k maka terlebih dahulu menentukan orde masing-masing pereaksi
Menentukan orde A : cari 2 [B] yang sama (percobaan 1 dan 2)
![]()
![]()
![]()
x = 0
Menentukan orde B : cari 2 [A] yang sama (percobaan 2 dan 3)
![]()
![]()
![]()
y = 2
maka persamaan laju reaksinya adalah v = k[B]2
Untuk menentukan k masukan ke salah satu percobaan (ambil percobaan 1)
v1 = k [B]1
![]()
Jawaban A
- Sama seperti semula
- Lebih besar 2 kali
- Lebih kecil 2 kali
- Lebih kecil 4 kali
- Lebih besar 4 kali
PEMBAHASAN :
Konsentrasi NO tidak akan mempengaruhi laju reaksi karena memiliki orde nol atau tidak ada dalam persamaan laju reaksi. Sedangkan jika konsentrasi Br dinaikan 2 kali maka laju reaksi menjadi:
![]()
v2 = 4v1
Laju reaksi yang baru lebih besar 4 kali dari laju reaksi semula
Jawaban E
A + B → C + D
Berdasarkan data diatas, tingkat reaksi total adalah …
- 0
- 1/2
- 1
- 2
- 3
PEMBAHASAN :
Untuk menentukan orde total maka terlebih dahulu menentukan orde masing-masing pereaksi
Menentukan orde A : cari 2 [B] yang sama (percobaan 1 dan 2)
![]()
![]()
![]()
x = 1
Menentukan orde B : cari 2 [A] yang sama (percobaan 4 dan 5)
![]()
![]()
![]()
y = 0
maka orde totalnya adalah x + y = 1 + 0 = 1
Jawaban C
Setiap kenaikan suhu 10◦C, laju reaksi menjadi dua kali lebih cepat dari semula. Jika pada suhu 20◦C laju reaksi berlangsung 8 menit, maka laju reaksi pada suhu 50◦C adalah …
- 1/2 menit
- 1/4 menit
- 1 menit
- 2 menit
- 4 menit
PEMBAHASAN :
Diketahui:
kenaikan suhu = 10 oC
kenaikan laju = 2x
T1 = 20 oC
T2 = 50 oC
Menentukan waktu reaksi saat 50 oC menggunakan rumusan:

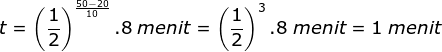
Jawaban C
Dari data tersebut faktor yang mempengaruhi laju reaksi tersebut adalah …
- Waktu
- Konsentrasi
- Luas permukaan
- Luas permukaan & waktu
- Konsentrasi & suhu
PEMBAHASAN :
Dari data yang diperoleh dari tabel konsentrasi HCl dibuat tetap artinya tidak akan mempengaruhi laju reaksi. Sedangkan yang diubah adalah luas permukaan dalam bentuk serbuk, butiran dan kepingan yang menyebabkan perubahan terhadap waktu reaksi. Maka faktor yang mempengaruhi adalah luas permukaan
Jawaban C
Soal No.9
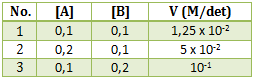
Jika [A] diubah menjadi 0,3 M dan [B] menjadi 0,4 M, maka nilai laju reaksi (v) pada saat itu adalah … M/det
- 5,4
- 7,2
- 9,6
- 18
- 36
PEMBAHASAN :
Untuk menentukan laju reaksi yang baru perlu mengetahui orde masing-masing pereaksi.
Menentukan orde A : cari 2 [B] yang sama (percobaan 1 dan 2)
![]()
![]()
![]()
x = 2
Menentukan orde B : cari 2 [A] yang sama (percobaan 1 dan 3)
![]()
![]()
![]()
y = 3
maka persamaan laju reaksinya adalah v = k[A]2[B]3
Untuk menentukan v saat [A] = 0,3 dan [B] = 0,4 maka ditentukan dari perbandingan dengan percobaan yang lain. Ambil percobaan 1
![]()
nilai k bisa di coret karena nilainya sama,maka:
![]()
v = 576 x 1,25 x 10-2 = 7,2
Jawaban B
Perlakuan apa saja yang tidak memberi pengaruh terhadap laju reaksi?
- Ukuran partikel- partikel pereaksi diperkecilkan
- Suhu di tingkatkan
- Konsentrasi pereaksi ditambahkan
- Volume pereaksi diperbesar
- Katalis ditambahkan kedalam reaksi
PEMBAHASAN :
Faktor-faktor yang mempengaruhi laju reaksi:
- Luas permukaan, jika ukuran partikel diperkecil maka luas permukaannya semakin besar semakin cepat bereaksi
- Suhu ditingkatkan menyebabkan energi kinetik zat meningkat sehingga reaksi semakin cepat.
- Konsentrasi pereaksi ditambah menyebabkan semakin banyak zat yang bertumbukan sehingga semakin cepat bereaksi.
- Katalis ditambahkan untuk menurunkan energi aktivasi sehingga reaksi semakin cepat.
Faktor yang tidak mempengaruhi yaitu volume pereaksi. Maka jawaban yang tepat adalah D
Jawaban D
DOWNLOAD KUMPULAN SOAL ULANGAN LAJU REAKSI DALAM BENTUK PDF KLIK DISINI