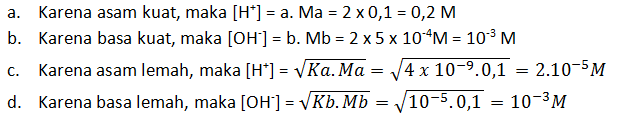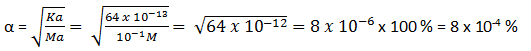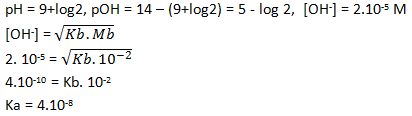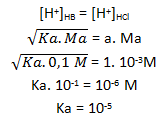Contoh Soal dan Pembahasan Asam Basa dan Titrasi
PEMBAHASAN :
Dengan menggunakan suatu alat yang dapat membedakan mana asam atau basa yang disebut indikator
DOWNLOAD CONTOH SOAL ASAM BASA DALAM BENTUK PDF KLIK DISINI
B. Jelaskan persyaratan suatu zat dapat digunakan sebagai indikator asam-basa
PEMBAHASAN :
A. suatu bahan atau alat yang dapat menentukan sifat asam / basa suatu larutan
B. persyaratan suatu zat dapat digunakan sebagai indikator yaitu memiliki warna yang berbeda ketika dimasukan ke dalam larutan asam atau ke larutan basa
LIHAT JUGA :
| Latihan Soal Asam Basa | Video Asam Basa | Tempat Nanya |
| Klik Disini | Klik Disini | Klik Disini |
| Rangkuman Asam Basa | Soal Ulangan Asam Basa | |
| Klik Disini | Klik Disini |
PEMBAHASAN :
Kembang sepatu
Kol ungu
Kunyit
Daun pandan
Bunga kertas
LIHAT JUGA : Video Pembelajaran Asam Basa
PEMBAHASAN :
Asam : Zat yang dimasukan ke dalam air akan menghasilkan ion H+
Contoh :
Asam
HCl → H+ + Cl-
Basa
NaOH → Na+ + OH-
Basa : Zat yang dimasukan ke dalam air akan menghasilkan ion OH-
a. CH3COOH(aq) →
b. H2CO3(aq) →
c. HNO3(aq) →
d. NH4OH(aq) →
e. Ca(OH)2 →
PEMBAHASAN :
a. CH3COOH(aq) → CH3COO-(aq) + H+(aq)
b. H2CO3(aq) → 2H+(aq) + CO32-(aq)
c. HNO3(aq) → H+(aq) + NO3(aq)
d. NH4OH(aq) → NH4+(aq) + OH-(aq)
e. Ca(OH)2 → Ca2+(aq) + 2OH-(aq)
PEMBAHASAN :
Asam lemah : asam yang derajat ionisasinya lebih kecil dibanding asam kuat atau kurang terurai dan sedikit menghasilkan ion H+ dalam larutannya
Asam kuat : asam yang derajat ionisasinya besar atau mudah terurai dan banyak menghasilkan ion H+ dalam larutannya
PEMBAHASAN :
Asam : pemberi/donor proton (H+)
Basa : penerima/akseptor proton (H+)
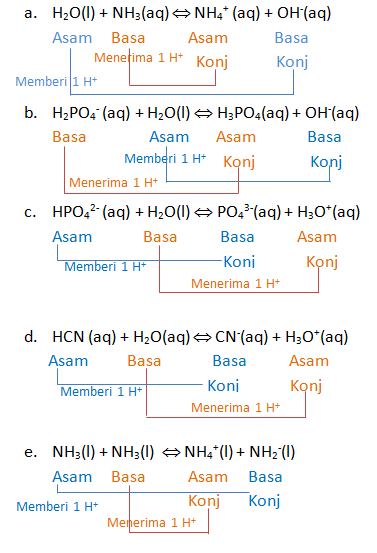
Tentukan spesi yang bertindak sebagai asam dan basa dan pasangan asam-basa konjugasinya
a. H2O(l) + NH3(aq) ⇔ NH4+ (aq) + OH‑(aq)
b. H2PO4- (aq) + H2O(l) ⇔ H3PO4(aq) + OH-(aq)
c. HPO42- (aq) + H2O(l) ⇔ PO43-(aq) + H3O+(aq)
d. HCN (aq) + H2O(aq) ⇔ CN-(aq) + H3O+(aq)
e. NH3(l) + NH3(l) ⇔ NH4+(l) + NH2-(l)
PEMBAHASAN :
Asam : Penerima/akseptor pasangan elektron
Basa : Pemberi/donor pasangan elektron
Contoh:
NH3 + BF3 → NH3BF3
Basa asam
NH3 memberikan pasangan elektron bebasnya ke BF3 yang tidak oktet
PEMBAHASAN :
Kelebihan Arrhenius : mampu menjelaskan proses netralisasi lebih baik dibanding teori-teori sebelumnya
Kelebihan Brosted-Lowry : Dapat menjelaskan basa yang tidak memiliki ion OH- dan tidak terbatas pada pereaksi air.
Kelebihan Lewis : Dapat menjelaskan asam yang tidak memiliki ion H+, dapat menjelaskan asam basa tanpa ada H+ dan OH-
a. CH3COOH
b. NaOH
PEMBAHASAN :
a. CH3COOH = bersifat asam. Basa konjugasinya adalah CH3COO-
b. NaOH = bersifat basa. Asam konjugasinya adalah Na+
PEMBAHASAN :
Bersifat asam dengan melepaskan 1H+
H2PO4- → HPO42-
Bersifat basa dengan menerima 1 H+
H2PO4- → PO42-
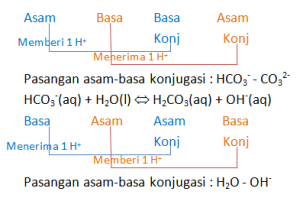
HCO3-(aq) + H2O(l) ⇔ CO32-(aq) + H3O+(aq)
HCO3-(aq) + H2O(l) ⇔ H2CO3(aq) + OH-(aq)
Tentukan pasangan asam-basa konjugasi pada reaksi di atas
CO2(g) + H2O(l) ⇔ H2CO3(aq)
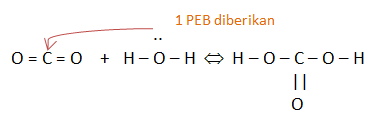
Gambarkan struktur Lewis dari reaksi tersebut. Jelaskan manakah molekul yang bertindak sebagai asam dan sebagai basa
Yang bertindak sebagai asam yaitu CO2 karena menerima pasangan elektron sedangkan yang bertindak sebagai basa yaitu H2O karena memberikan 1 pasangan elektron
PEMBAHASAN :
Tidak mampu menjelaskan reaksi asam basa yang tidak melibatkan proton (H+)
PEMBAHASAN :
Kw = [H+].[OH-]
10-12 = [H+].[OH-]
Reaksi swaionisasi air
H2O ⇔ H+ + OH-
Karena koefisiennya sama maka, [H+] = [OH-]
10-12 = [H+].[H+]
10-12 = [H+]2
Maka [OH-] = 10-6 M
a. Larutan H2SO4 0,1 M
b. 100 mL larutan Ba(OH)2 5 x 10-4 M
c. Larutan HBrO 0,1 M Ka = 4 x 10-9
d. Larutan NH3 0,1 M Kb = 10-5

Tentukan:
a. Asam yang paling kuat dan yang paling lemah
b. Urutan kekuatan asam dari yang paling lemah ke yang paling kuat
PEMBAHASAN :
- Rumusan [H+] untuk asam lemah yaitu [H+] = , dimana nilai Ka berbanding lurus dengan [H+], semakin besar Ka maka [H+] semakin besar artinya semakin kuat asamnya begitu pula sebaliknya. Jadi untuk menentukan mana yang paling kuat berarti Ka yang paling besar yaitu HIO3 (Ka = 1,6 x 10-1). Sedangkan yang paling lemah berarti nilai Ka nya kecil yaitu HbrO (Ka = 2,3 x 10-9)
- Asam dari yang paling lemah ke yang paling kuat (Ka kecil ke Ka besar)
HBrO – C6H5COOH – HF – HClO2 – HIO3
a. Ba(OH)2 0,0005 M
b. HCl 0,02 M
c. CH3COOH 0,1 M (Ka = 10-5)
d. NH3 0,1 M (Kb = 10-5)
e. HF 0,1 M (Ka = 8,1 x 10-4)
PEMBAHASAN :
Misal :
Volume HCl = v mL
Volume H2SO4 = v mL
maka nH+total = nH+1 + nH+2
nH+1 dari HCl
nH+1 = a . Ma. V = 1 x 10-1 . V = 10-1 V
nH+2 dari H2SO4
nH+2 = a . Ma.V = 2 x 10-1 V
nH+total = nH+1 + nH+2 = 0,1V + 0,2V = 0,3V
[H+] = n/V total = 0,3 V/ (V +V) = 0,3/2 = 0,15 = 1,5 x 10-1
pH = 1 – log 1,5
PEMBAHASAN :
Agar warna larutan berwarna HIn maka pH larutan harus lebih kecil dari pKa dan jika ingin berwarna In- maka pH larutan harus lebih besar dari pKa. Jika Ka = 10-5 maka pKa nya = 5. Untuk berwarna merah (HIn) maka pHnya harus lebih kecil dari 5 (pH < 5). Sedangkan untuk berwarna kuning (In-) maka pHnya harus lebih besar dari 5 (pH > 5)
PEMBAHASAN :
Jika menghasilkan warna yang sama maka pH kedua larutan sama, artinya [H+] nya sama
PEMBAHASAN :
Dengan penambahan Metil merah = Jingga artinya pHnya diantara 4,4 – 6,2 (perpaduan warna)
Dengan penambahan metil jingga = kuning, artinya pHnya > 4,4
Jika dibuat diagramnya

pH berada pada rentang : 4,4 < pH < 6,2
Jika ditambah BTB maka akan ada dua kemungkinan:
Jika pHnya < 6 maka berwarna kuning
Jika pHnya 6 < pH < 6,2 maka warnanya akan hijau
a. CH3COOH 0,1 M (Ka = 10-5)
b. NaOH 0,01 M
c. Air murni
- Apa warna larutan CH3COOH 0,1 M ( Ka = 10-5) jika ditetesi ketiga indikator di atas?
- Jika suatu larutan berwarna hijau dengan penambahan BTB. Apa larutan tersebut jika ditambah PP
- Jika suatu larutan ditambah metil jingga berwarna merah, apa warna larutan jika ditetesi bromtimol biru?
PEMBAHASAN :
pH sebelum dicampur
pH H2SO4 (asam kuat)
[H+] = a. Ma = 2 . 10-1 M
pH = 1 – log 2
pH KOH (basa kuat)
[OH-] = b. Mb = 1 . 10-1 M
pOH = 1, pH = 14 – 1 = 13
PH sesudah dicampur
n H2SO4 = M x V = 0,1M x 100 ml = 10 mmol
n KOH = M x V = 0,1M x 100 ml = 10 mmol
PEMBAHASAN :
[H+] dari larutan dengan pH = 1 yaitu 10-1 M
[OH-] dari larutan dengan pH = 13 atau pOH = 14 -13 = 1 yaitu 10-1 M
Reaksikan H+ dengan OH-
nH+ = M x V = 10-1 x 100 ml = 10 mmol
nOH- = M x V = 10-1 x 50 ml = 5 mmol
PEMBAHASAN :
Menggunakan rumus netralisasi
a.Ma. Va = b. Mb. Vb
2.0,5M. 50 ml = 1. 1 M. Vb
Vb = 50 ml
PEMBAHASAN :
Menggunakan rumus netralisasi
a.Ma.Va = b. Mb.Vb
1. Ma. 5 mL = 2 . 0,001 M. 20 mL
Ma = 0,04/5 = 0,008 M
PEMBAHASAN :
Menggunakan rumus netralisasi
a.Ma.Va = b.Mb. Vb
1.0,05 M. 10 mL = 2. Mol basa
Mol b = 0,25 mmol
Gr = mol x Mr = 0,25 mmol x 74 = 18,5 mgram = 0,0185 gram
PEMBAHASAN :
PEMBAHASAN :
Menggunakan rumus netralisasi
a.Ma.Va =b.Mb.Vb
2.0,1 M. 10 mL = 1. Mb. 50 mL
Mb = 2/50 = 0,04 M
PEMBAHASAN :
Menggunakan rumus netralisasi
a.Ma.Va =b.Mb.Vb
2. 0,3 M. 25 cm3 = 1. 0,1 M. Vb
Vb = 15/0,1 = 150 cm3
Reaksi yang terjadi:
Mol NaOH = M x V = 0,3 M . x cm3 = 0,3x mmol
Mol MgCl2 = M x V = 0,2 M . 75 cm3 = 15 mmol
Agar tepat habis bereaksi maka NaOH & MgCl2 harus habis
Mula2 0,3 x 15 - -
Reaksi 0,3x 0,15x - 0,15x 0,3x +
Sisa - 15 – 0,15x 0,15x 0,3x
15 – 0,15x = 0 (habis bereaksi)
15 = 0,15x
x =15/0,15 =100 cm3 (volume NaOH)
Menentukan gram Mg(OH)2
n Mg(OH)2 = 0,15x = 0,15.100 = 15 mmol = 0,015 mol
Gr = n x Mr = 0,015 mol x 58 = 0,87 gram
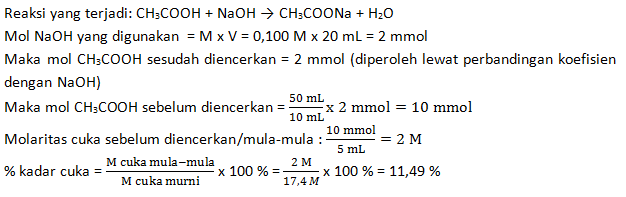
PEMBAHASAN
Menggunakan rumus titrasi
a.Ma.Va = b.Mb.Vb
0,1 M. 25 mL = 1. Mb. 29 mL
Mb = 2,5/ 29 = 0,086 M
Fe(s) + 2HCl(aq) → FeCl2(aq) + H2(g)
Sumber Soal : Kelas XI Penerbit Erlangga Pengarang Unggul Sudarmo
DOWNLOAD CONTOH SOAL ASAM BASA DALAM BENTUK PDF KLIK DISINI
LIHAT JUGA :
| Latihan Soal Asam Basa | Video Asam Basa | Tempat Nanya |
| Klik Disini | Klik Disini | Klik Disini |
| Rangkuman Asam Basa | Soal Ulangan Asam Basa | |
| Klik Disini | Klik Disini |