Kumpulan Soal Ulangan Asam Basa Dengan Pembahasannya
PEMBAHASAN :
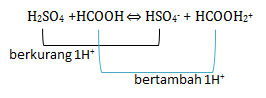
Pasangan asam- basa konjugasi adalah teori yang di cetuskan oleh Bronsted-Lowry. Dimana asam adalah zat yang memberikan/donor proton(H+) sehingga di akhir akan berkurang 1 H+. Sedangkan basa adalah penerima/akseptor proton(H+) sehingga di akhir akan bertambah 1H+. Jika dilihat dari reaksinya:
H2SO4 berkurang 1H+ menjadi HSO4- sehingga H2SO4 bersifat asam sedangkan HSO4- akan bersifat basa atau menjadi basa konjugasi
HCOOH bertambah 1H+ menjadi HCOOH2+ sehingga HCOOH bersifat basa sedangkan HCOOH2+ akan bersifat asam atau menjadi asam konjugasi
Maka pasangan asam-basa konjugasinya adalah H2SO4 - HSO4-
DOWNLOAD KUMPULAN SOAL ASAM BASA & PEMBAHASANNYA DALAM BENTUK PDF KLIK DISINI
LIHAT JUGA :
| Latihan Soal Asam Basa | Video Asam Basa | Tempat Nanya |
| Klik Disini | Klik Disini | Klik Disini |
| Rangkuman Asam Basa | Contoh Soal Asam Basa | |
| Klik Disini | Klik Disini |
PEMBAHASAN :
Mr H2SO4 = (1 x 2 + 32 x 1 + 16 x 4) = 98
Menentukan molaritas H2SO4
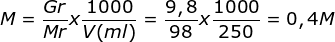
Menentukan pH
Karena H2SO4 merupakan asam kuat maka rumusannya:
[H+] = a. Ma = 2. 0,4 M = 0,8 M = 8 x 10-1 M
pH = - log[H+] = - log 8 x 10-1 M = 1 - log 8
PEMBAHASAN :
NH4OH merupakan basa lemah sehingga terionisasi sebagian. Untuk menentukan derajat ionisasinya menggunakan rumusan:
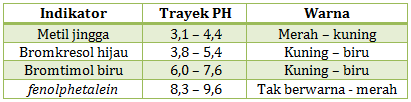
Diketahui trayek perubahan warna indikator sebagai berikut:
- terhadap indikator metil jingga memberi warna kuning
- terhadap indikator bromkresol hijau memberi warna biru
- terhadap indikator bromtimol biru memberi warna biru
- terhadap indikator fenolphtalein tidak memberi warna.
Perkiraan pH sampel air tersebut adalah….
PEMBAHASAN :
Dalam mengerjakan soal ini cukup melihat posisi warna yang diperlihatkan dengan pH nya. Jika warna yang diperlihatkan berada di kanan, maka pHnya di atas angka yang kanan. Jika warna yang diperlihatkan di kiri maka pHnya di bawah angka yang kiri. Jika warnanya perpaduan warna kiri kanan. maka PH nya berada di rentan angka kiri kanan.
- sampel air dengan metil jingga memberi warna kuning artinya pH di atas 4,4
- sampel air dengan bromkresol hijau memberi warna biru artinya pH di atas 5,4
- sampel air dengan bromtimol biru memberi warna biru artinya pH di atas 7,6
- sampel air dengan metil fenolphtalein tidak memberi warna artinya pH di bawah 8,3
Jika lebih darinya ada lebih dari satu ambil angka yang terbesar. Dari data tersebut lebih darinya ada 3 yaitu diatas 4.4, di atas 5.4, di atas 7.6. Sehingga diambil diatas 7.6 dan di bawah 8.3. jika dituliskan menjadi
7.6 < pH < 8.3
PEMBAHASAN :
K2O merupakan oksida basa. Jika direaksikan dengan air maka akan menghasilkan larutan basa KOH.
K2O + H2O → 2KOH
Dalam netralisasi berlaku
mol H+ = mol OH+
a.Ma.Va = b.Mb.Vb (a = valensi asam/jumlah H+, b = valensi basa/jumlah OH-)
2. 0,1 M. 30 ml = 1. Mb. 25 ml
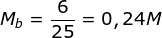
n KOH = M x V = 0,24 x 1 L = 0,24 mol
n K2O = 1/2 x 0,24 mol = 0,12 (dihitung lewat perbandingan dengan koefisien)
Gr K2O = n x Mr = 0,12 x 94 = 11,28 gr
Maka kadarnya:
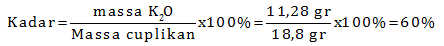
PEMBAHASAN :
Dalam reaksi penetralan berlaku:
mol H+ = mol OH-
Karena H+ berasal dari dua zat asam yaitu HBr dan H2SO4 maka perlu dicari mol H+ total
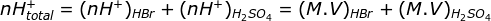
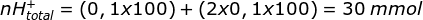
Dalam menentukan mol H+ dari H2SO4 dikali 2 karena valensi asamnya/jumlah H+ nya = 2
maka volume basanya
mol H+ = mol OH-
30 mmol = b.Mb.Vb
30 =1. 0,2 M. Vb
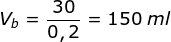
PEMBAHASAN :
Dalam netralisasi berlaku:
mol H+ = mol OH-
a.Ma.Va = b.Mb.Vb
1. 0,4 M. 100 = 2. n ( n = Mb. Vb)
n = 20 mmol = 2 x 10-2 mol
Menentukan Mr menggunakan rumusan
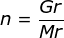
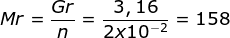
Menentukan Ar M
Mr M(OH)2 = Ar M x 1 + Ar O x 1 + Ar H x 2
158 = Ar M + 16 + 1 x 2
Ar M = 158 - 18 = 140
PEMBAHASAN :
Menentukan asam konjugasi berarti HCO3- nya sendiri bersifat basa. Pertanyaan ini berdasarkan teori asam basa Bronsted-Lowry. Basa menurut Bronsted-Lowry merupakan penerima proton (H+) sehingga untuk menentukan asam konjugasinya maka basa perlu ditambah 1H+. Sehingga Asam konjugasi dari HCO3- adalah H2CO3
PEMBAHASAN :
CaO merupakan oksida basa yang jika direaksikan dengan air akan menghasilkan basanya
CaO + H2O → Ca(OH)2
Menentukan mol masing-masing
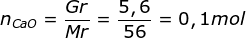
n Ca(OH)2 akan sama dengan nCaO karena koefisiennya sama
nCa(OH)2 = 0,1 mol
Mereaksikan Ca(OH)2 dengan HCl
mol HCl = 0,1 M x 1 l = 0,1 mol
Ca(OH)2 + 2HCl → CaCl2 + 2H2O
mula2 0,1 0,1 - -
reaksi 0,05 0,1 - 0,05 0,1 +
sisa 0,05 - 0,05 0,1
Karena yang bersisa adalah Ca(OH)2 maka pH campuran akan bersifat basa, karena termasuk basa kuat maka rumusannya

[OH-] = b.Mb = 2. 0,05 M = 0,1 M = 10-1 M
pOH = 1
pH = 14 - 1 = 13
PEMBAHASAN :
Karena NaOH merupakan basa maka pH kita ubah ke pOH
pOH = 14 - pH = 14 - 12 = 2
[OH-] = 10-2
Karena basa kuat maka rumusannya
[OH-] = b. Mb
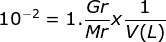
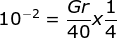
Gr = 160 x 10-2 = 1,6 gram
DOWNLOAD KUMPULAN SOAL ASAM BASA & PEMBAHASANNYA DALAM BENTUK PDF KLIK DISINI
LIHAT JUGA :
| Latihan Soal Asam Basa | Video Asam Basa | Tempat Nanya |
| Klik Disini | Klik Disini | Klik Disini |
| Rangkuman Asam Basa | Contoh Soal Asam Basa | |
| Klik Disini | Klik Disini |