Update Terbaru? Gabung Disini : facebook_accounttwitter_accountgoogle_plus_accountyoutube_account
Sifat Koligatif Larutan Elektrolit dan Non Elektrolit
Rangkuman Materi Sifat Koligatif
KONSENTRASI
- Banyaknya zat terlarut dalam sejumlah zat pelarut.
1. Fraksi mol (X)
Menyatakan perbandingan jumlah mol komponen suatu zat terhadap total mol semua komponen yang terdapat dalam larutan
Jika larutan hanya terdiri dari dua komponen, zat A dan zat B, berlaku:
XB = 1 - XA
2. Molalitas (m)
Banyaknya zat terlarut di dalam satu kilogram pelarut.
P = berat pelarut
3. Molaritas (M)
Banyaknya zat terlarut di dalam satu liter larutan.
V = volume larutan
DOWNLOAD RANGKUMAN SIFAT KOLIGATIF DALAM BENTUK PDF Klik Disini
SIFAT KOLIGATIF
- Pengertian
Sifat larutan yang tidak bergantung pada jenis zat terlarut, tetapi bergantung pada konsentrasi/jumlah partikel zat terlarut.
LIHAT JUGA : Contoh Soal & Pembahasan Sifat Koligatif Bagian I
1. Penurunan Tekanan Uap (∆P)
-
Tekanan yang ditimbulkan oleh uap yang terbentuk dari zat cair yang berubahmembentuk fasa gas.
-
Penambahan zat terlarut non volatile(sukar menguap) dapat menyebabkanmenurunkan tekanan uap. Karena partikel pelarut akan terhalang ketika akanmenguap.

-
Jika tekanan uap pelarut (Po) dan tekanan uap larutan (PL). Maka berlaku :
Po > PL
-
Besar penurunannya (∆P) adalah :
∆P = Po - PL
-
Hubungan penurunan tekanan uap (∆P) dengan fraksi mol (X)
Francois M. Raoult menjelaskan hubungan PL dengan X melalui hukum Raoult dalam
persamaan :PL = XP . Po
Xp = fraksi mol pelarut
Karena Xp + Xt = 1, maka diperoleh rumusan:
∆P = Xt . Po
Xt = fraksi mol terlarut
LIHAT JUGA : Video Pembelajaran Sifat Koligatif
2. Kenaikan Titik Didih (∆Tb)
-
Akibat tekanan uap larutan mengalami penurunan dari tekanan uap pelarut, maka titikdidih larutan akan lebih tinggi dibandingkan titik didih pelarut.
-
Dengan penambahan zat terlarut. Titik didih larutan akan lebih tinggi dibandingkantitik didih pelarut. Hal ini dapat dijelaskan dengan diagram fasa:

-
Jika titik didih pelarut (Tbo) dan titik didih larutan (TbL). Maka berlaku :
Tbo < TbL
Besar kenaikan titik didih (∆Tb) adalah :
∆Tb = Tb
L - Tbo
Tbo air = 100oC
Tb L > 100oC
- Hubungan kenaikan titik didih dengan konsentrasi (molalitas):
∆Tb = Kb . m
Kb = Tetapan Kenaikan titik didih molal
(air = 0,52oC/m)
LIHAT JUGA : Contoh Soal Sifat Koligatif Bagian II
3. Penurunan Titik Beku (∆Tf)
-
Dengan penambahan zat terlarut. Titik beku larutan akan lebih rendah dibandingkantitik beku pelarut. Hal ini dapat dijelaskan dengan diagram fasa.
-
Jika titik beku pelarut (Tfo) dan titik beku larutan (TfL). Maka berlaku :
Tfo > TfL
Besar penurunan titik beku (∆Tf) adalah :
∆Tf = Tf o– Tf L
Tfo air = 0oC
Tb L < 0oC
- Hubungan penurunan titik beku dengan konsentrasi (molalitas):
∆Tb = Kb . m
Kb = Tetapan Kenaikan titik didih molal
(air = 0,52oC/m)
4. Tekanan osmosis (π)
-
Osmosis adalah proses perpindahan larutan yang memiliki konsentrasi rendahmelalui membran semipermeabel menuju larutan yang memiliki konsentrasilebih tinggi hingga tercapai kesetimbangan konsentrasi.
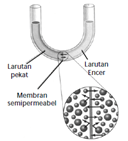
-
Tekanan yang diterapkan untuk menghentikan proses osmosis dari larutan enceratau pelarut murni ke dalam larutan yang lebih pekat disebut tekanan osmotik larutan.
-
Rumusan tekanan osmosis:
π = M.R.T
Keterangan:
π = Tekanan Osmosik
M = Molaritas
R = Tetapan Gas Umum (0,082 L atm/k mol)
-
Sifat Koligatif larutan elektrolit
Perbedaan jumlah partikel larutan elektrolit dan larutan non elektrolit menyebabkannilai sifat koligatif menjadi berbeda. Rumusan sifat koligatif untuk larutan elektrolitharus dikalikan faktor Van Hoff (i)
i = (1 + (n-1)α)
Ket: n = jumlah ion , α= derajat ionisasi
Rumusan Sifat Koligatif Larutan Elektrolit:
|
∆P |
∆Tb |
∆Tf |
π |
|
∆P = Xt . Po
|
∆Tb = Kb . m . i |
∆Tf = Kf . m . i |
π = M . R . T. i |
DOWNLOAD RANGKUMAN SIFAT KOLIGATIF DALAM BENTUK PDF Klik Disini
KINI HADIR LAYANAN BERTANYA TUGAS & PR PREMIUM (FAST RESPOND!!)
CUKUP PAKAI FASILITAS SMS, WA atau BBM Dan PR Mu Terbantu Dengan Cepat
Hanya Rp. 5.000 (Lima Ribu Rupiah) Per soal yang ditanyakan.
Mata pelajaran yang bisa ditanyakan Kimia, Fisika, Biologi, Matematika. (Tingkat SMP & SMA).
Misal kamu mau nanya 3 soal berarti tinggal di kali Rp. 5 rb Jadi totalnya 15 rb
Dana bisa di transfer ke rekening BNI 0360871320 an Yudi Syarif H
Pertanyaan akan kami layani sesudah menunjukan bukti transfer lewat WA dengan no HP ada di bawah
Dijawab oleh guru yang sudah ahli di bidangnya
Layanan Bantuan PR/Tugas dari jam 14.00 s.d 21.30 WIB
(menghindari kecurangan saat ujian)
INFORMASI LEBIH LANJUT HUB : 089622667471 (SMS / WA)
thanks.. sangat membantu
terimakasih. sangat membantu. semoga terus sukses !
sama-sama heni