DAFTAR ISI
Pengertian Atom
Atom Merupakan partikel terkecil yang sudah tidak dapat dibagi-bagi lagi dengan cara biasa
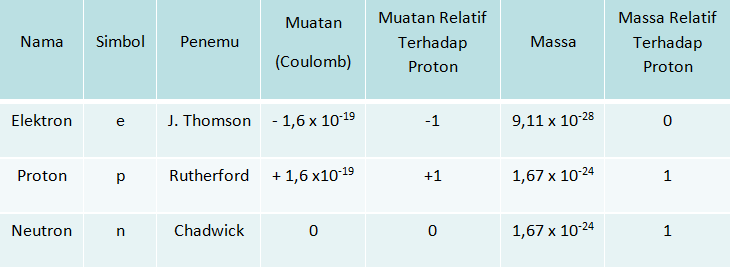
Partikel Penyusun Atom
Nomor Atom dan Massa Atom
Nomor atom (Z) menunjukkan jumlah proton dalam atom.
- Untuk atom netral(tidak bermuatan) jumlah proton (p) = jumlah elektron (e)
- Untuk ion negatif (anion) jumlah proton (p) < jumlah elektron (e)
- Untuk ion positif (kation) jumlah proton (p) > jumlah elektron (e),
Massa atom (A) menunjukkan jumlah dari proton (p) dan neutron (n).
A = p + n
DOWNLOAD RANGKUMAN STRUKTUR DAN MODEL ATOM DALAM BENTUK PDF KLIK DISINI
Notasi Atom
X = Unsur/atom
A = Massa Atom/Nomor Massa = p + n
n = A - p
Z = Nomor Atom = p = e (atom netral)
Contoh Soal
Tentukan nilai A, Z, p, e, n untuk atom berikut :
a.
b.
Jawaban
a. A =23, Z = 11, p = 11, e = 11, n =23-11 = 12
b. A =19, Z = 9, p = 9, e = 9, n = 19 – 9 = 10
LIHAT JUGA :
| Latihan Soal Struktur Atom | Video Struktur Atom | Tempat Nanya |
| Klik Disini | Klik Disini | Klik Disini |
| Rangkuman Atom Modern | Contoh Soal I | |
| Klik Disini | Klik Disini |
Notasi Ion
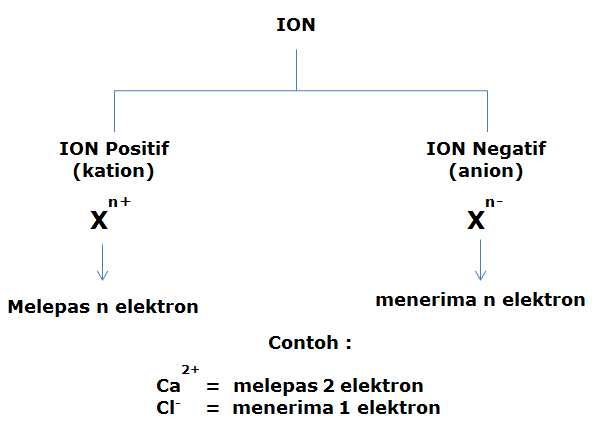
Contoh Soal:
Tentukan nilai A, Z, p, e, n untuk ion berikut :
a.
b.
Jawaban:
a. A =23, Z = 11, p =11, e = 11-1 = 10, n = 23 – 11 = 12 (melepas 1 elektron)
b. A =16, Z = 8, p =8, e = 8+2 = 10, n = 16 – 8 = 8 (menerima 2 elekron)
Perkembangan Model Atom
Model Atom Dalton
Atom merupakan partikel terkecil suatu materi yang berbentuk bola pejal.
- Atom suatu unsur memiliki sifat yang sama, berbeda dengan unsur yang lain
- Atom dapat bergabung dengan atom lain membentuk suatu molekul dengan perbandingan sederhana.
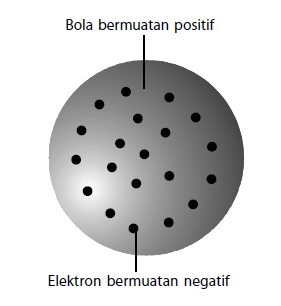
Model Atom Thomson
Atom merupakan bola yang bermuatan positif dan di dalamnya tersebar elektron yang bermuatan negatif.
- Model ini timbul karena ditemukannya elektron dalam atom.
- Model ini disebut juga teori Roti Kismis, karena mirip dengan roti kismis.
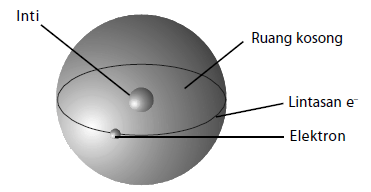
Model Atom Rutherford
Atom terdiri atas inti yang bermuatan positif dan dikelilingi oleh elektron.
- Model ini lahir karena Rutherford menemukan adanya inti atom melalui percobaannya.
- Kelemahannya yaitu ketidakmampuan menjelaskan mengapa elektron tidak jatuh ke inti akibat gaya tarik elektrostatik
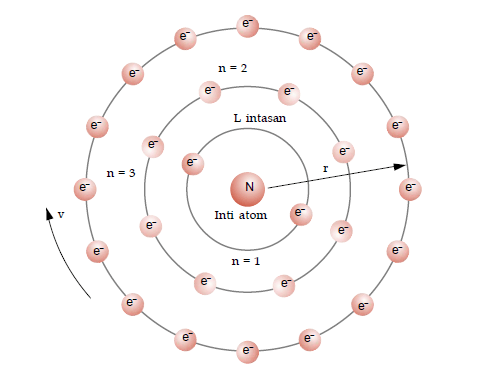
Model Atom Niels Bohr
Atom terdiri atas inti yang terdiri atas proton dan neutron dan dikelilingi oleh elektron pada lintasan dengan tingkat energi yang tetap.
- Elektron dapat berpindah ke tingkat energi yang lebih tinggi (kulit yang lebih besar) dengan menyerap energi, dan sebaliknya.
- Elektron dapat berpindah ke tingkat energi yang lebih tinggi (kulit yang lebih besar) dengan menyerap energi, dan sebaliknya.
DOWNLOAD RANGKUMAN STRUKTUR DAN MODEL ATOM DALAM BENTUK PDF KLIK DISINI
LIHAT JUGA :
| Latihan Soal Struktur Atom | Video Struktur Atom | Tempat Nanya |
| Klik Disini | Klik Disini | Klik Disini |
| Rangkuman Atom Modern | Contoh Soal I | |
| Klik Disini | Klik Disini |