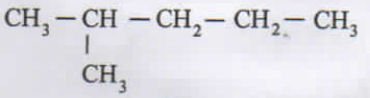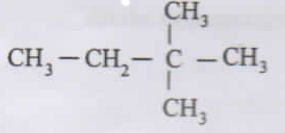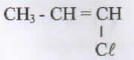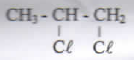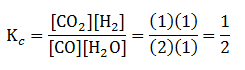Pembahasan Soal Ujian Nasional (UN) SMA Kimia 2014
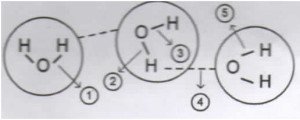
Ikatan antar molekul terjadi diantara 2 molekul. Untuk no, 1, 2, 3 dan 5 disebut ikatan intra molekul. Yang termasuk ikatan intra molekul yaitu ikatan ion dan kovalen. Sedangkan ikatan no.4 termasuk ikatan antar molekul. yang termasuk ikatan antar molekul yaitu gaya van der waals (gaya dipol, gaya dipol terimbas & gaya london) dan ikatan hidrogen
JAWABAN D
Konfigurasi elektron dan letak unsur V dalam table periodik adalah…
- [Ar]4s2 3d3 Gol IIIB Periode 3
- [Ar]3d3 4s2 Gol VA Periode 3
- [Ar]4s1 3d4 Gol IVB Periode 4
- [Ar]3d2 4s2 5s2 Gol IV A Periode 5
- [Ar]3d3 4s2 Gol VB Periode 4
PEMBAHASAN :
Jumlah elektron yaitu sama dengan nilai Z yaitu angka di bawah = 23
Jika dikonfigurasikan menggunakan gas mulia maka digunakan gas mulia Ar yang nomor atomnya di bawah 23.
maka konfigurasi dengan disingkat:
[Ar]3d3 4s2
karena berhenti di subkulit d maka termasuk golongan B, golongan B ditentukan dari jumlah elektron dari 4s = 2 dan 3d = 3, jadi 2+3 = 5, sehingga termasuk golongan V B dan Periode dilihat dari kulit terluar yaitu kulit 4 jadi termasuk periode 4, jadi jawabannya:
Gol VB Periode 4
JAWABAN E
LIHAT JUGA : Try Out Online UN Kimia
- tetrahedral dan nonpolar
- linear dan polar
- segiempat planar dan polar
- oktahedral dan nonpolar
- linear dan nonpolar
PEMBAHASAN :
Konfigurasikan masing-masing atom
4X : 2 2 (melepas 2 e) membentuk X2+
17Y : 2 8 7 (menangkap 1 e) membentuk Y–
Jika keduanya berikatan maka akan melakukan ikatan ion (terjadi antara yang melepaskan e (ion +) dengan yang menangkap e (ion -) membentu senyawa XY2. Karena memebntuk ikatan ion, seharusnya tidak ada istilah polar atau non polar. Tapi karena senyawa ion juga memiliki kutub (polar) maka senyawa ini bersifat polar. Bentuk molekulnya yaitu linear dengan atom pusat X dikelilingi oleh dua atom Y
Y – X – Y
JAWABAN E
LIHAT JUGA : Video Pembahasan UN Kimia 2014
(1).CH4
(2).PCl5
(3).NH3
(4).CHCl3
(5).H2O
Jika diketahui nomor atom H=1,C=6,N=7,O=8,P=15,Cl=17, senyawa yang tidak mengikuti aturan oktet adalah…
- 3
- 2
- 4
- 1
- 5
PEMBAHASAN :
senyawa yang tidak mengikuti kaidah oktet yaitu bisa terdiri dari atom yang berikatan namun kurang dari 8 atau lebih dari delapan. yang termasuk kurang dari delapan yaitu BF3 dan BeCl2. Sedangkan yang termasuk senyawa yang melebihi aturan oktet yaitu PCl5 dan SF6
JAWABAN B
LIHAT JUGA : Video Pembahasan UN Kimia 2015
| Percobaan | massaCu (g) | Massa S (g) | Massa CuS (g) |
| 1 | 4 | 2 | 6 |
| 2 | 6 | 2 | 6 |
| 3 | 8 | 4 | 12 |
| 4 | 8 | 10 | 12 |
Bedasarkan data percobaan tersebut maka perbandingan massa Cu dan S dalam senyawa CuS adalah..
- 2:1
- 4:5
- 3:1
- 1:3
- 1:2
PEMBAHASAN :
Untuk menentukan perbandingan massa Cu dan S dengan cara mudah yaitu dengan menjumlahkan massa Cu dan S dan jumlahnya tersebut harus sama dengan massa CuS. Untuk percobaan 1, penjumlahan massa Cu dan S sama dengan massa CuS, maka perbandingannya bisa ditentukan dari perbandingan massa Cu dan massa S
(Perc 1) Massa Cu : Massa S = 4 : 2 = 2: 1
JAWABAN A
CaCO3(s) + HCl(aq) → CaCl2(aq) + H2O(l) + CO2(g) (belum setara)
Volume gas yang dihasilkan jika diukur dalam keadaan standar sebanyak…(Ar C=12,O=16,Ca=40)
- 2,24 L
- 4,48 L
- 11,2 L
- 6,72 L
- 3,36 L
PEMBAHASAN :
Kita setarakan terlebih dahulu
CaCO3(s) + 2HCl(aq) → CaCl2(aq) + H2O(l) + CO2(g)
menentukan massa batu kapur (CaCO3)
![]()
menentukan mol gas CO2 dapat ditentukan dari perbandingan koefisien:
![]()
maka volume pada keadaan standar (STP):
V = n x 22,4 = 0,1 x 22,4 L = 2,24 L
JAWABAN A
- C3H8(g) → 3CO2(g) + 4H2O(g)
- C3H8(g) + O2(g) → CO2(g) + H2O(g)
- C3H8(g) + O2(g) → 3CO2 + 4H2O(g)
- C3H8(g) → CO2(g) + H2O(g)
- C3H8(g) + 5O2(g) → 3CO2 + 4H2O(g)
PEMBAHASAN :
Propana yaitu : C3H8, dibakar berarti direaksikan dengan O2, kemudian disetarakan:
Reaksi awal : C3H8(g) + O2(g) → CO2 + H2O(g)
Jumlah C : 3 1 x 3 (3 jadi koef CO2)
Jumlah H : 8 2 x 4 (4 jadi koef H2O)
Jumlah O 2x 5 (5 jadi koef O2) 10
Hasil penyetaraan:
C3H8(g) + 5O2(g) → 3CO2 + 4H2O(g)
JAWABAN E
NH3(aq) + HCl(aq) → NH4Cl(aq)
Harga pH larutan yang terjadi adalah.. (Kb NH3=10-5)
- 7+log 1
- 5-log 1
- 9+log 1
- 13-log 2
- 13+ log 2
PEMBAHASAN :
mol HCl = M x V = 0,2 x 25 ml = 5 mmol
mol NH3 = M x V = 0,2 x 25ml = 5 mmol
Reaksinya NH3(aq) + HCl(aq) → NH4Cl(aq)
M 5 5 –
R 5 5 – 5 +
S – – 5
Karena yang tersisa adalah garam saja. maka reaksi ini termasuk ke dalam hidrolisis. Karena garamnya berasal dari asam kuat dan basa lemah maka garamnya mengikuti yang kuat yaitu garam asam,
Mgaram = n/V = 5 mmol/(25+25) ml = 0,1 M
![]()
![]()
pH = 5 atau 5 -log 1
JAWABAN B
- 10-2 M
- 10-1 M
- 10-4 M
- 10-3 M
- 10-5 M
PEMBAHASAN :
Reaksikan terlebih dahulu antara NaOH dan CH3COOH:
Reaksi: NaOH + CH3COOH → CH3COONa + H2O
M 0,8 0,8 – –
R 0,8 0,8 0,8 0,8
S – – 0,8 0,8
Akan membentuk garam yang bersifat basa, kemudian menentukan [OH–] dari rumusan hidrolisis
Mgaram = n/v = 0,8/(100+100)ml = 0,004
![]()
![]()
Pada keadaat tepat jenuh Qsp = Ksp
Ca(OH)2 ⇔ Ca2+ + 2OH–
Ksp = [Ca2+][OH–]2
4×10-16 = [Ca2+].(2.10-6)2
[Ca2+] = 4×10-16/4.10-12
[Ca2+] = 10-4 M
JAWABAN C
(1) sinar matahari kelihatan saat masuk ruangan melalui celah
(2) pembentukan delta di muara sungai
(3) penjernihan air
(4) menggunakan alat cottrel dalam industri
(5) proses cuci darah
Penerapan sifat koloid dari elektroforesis dan dialisis secara berturut-turut adalah…
- (1) dan (2)
- (2) dan (3)
- (3) dan (4)
- (4) dan (5)
- (5) dan (1)
PEMBAHASAN :
(1) sinar matahari kelihatan saat masuk ruangan melalui celah merupakan contoh dari efek tyndall yaitu penghamburan cahaya oleh partikel koloid
(2) pembentukan delta di muara sungai merupakan contoh dari koagulasi yaitu proses penggumpalan dari sistem koloid karena adanya ion lain yang berbeda muatan
(3) penjernihan air merupakan contoh dari adsorpsi, yaitu proses penyerapan di bagian permukaan koloid. Penjernihan air dilakukan dengan menambahkan tawas atau alumunium sulfat
(4) menggunakan alat cottrel dalam industri merupakan contoh dari elektroforesis yaitu pergerakan partikel koloid dalam medan listrik.
(5) proses cuci darah merupakan contoh dari dialisis yaitu penyaringan ion-ion pengganggu melalui selaput semipermeabel
JAWABAN D
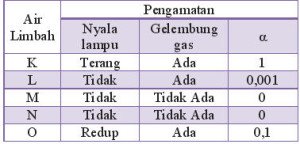
Pasangan air limbah yang bersifat elektrolit kuat dan non elektrolit adalah…
- K dan M
- K dan L
- L dan M
- L dan O
- L dan N
PEMBAHASAN :
Ciri elektrolit kuat:
– Nyala lampu terang
– Gelembung banyak
– derajat ionisasi (α) =1
Ciri elektrolit lemah:
– nyala lampu redup/mati
– gelembung sedikit
– derajat ionisasi 0<α<1
Ciri non elektrolit:
– nyala lampu mati
– tidak ada gelembung
– α = 0
JAWABAN A
- 2,47
- 2,70
- 2,40
- 3,41
- 3,20
PEMBAHASAN :
Menentukan mol HCl yang telah ditiupkan ke air melalui persamaan gas ideal:
PV = nRT
![]()
![]()
Menentukan molaritas HCl
![]()
pH = 3 – log 2 = 3 – 0,3 = 2,7
JAWABAN B
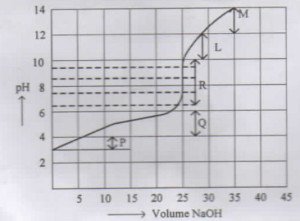
Daerah kurva yang merupakan larutan penyangga adalah…
- Q
- R
- P
- L
- M
PEMBAHASAN :
Pada daerah P perubahan pH dari 3 ke 4 dengan penambahan volume NaOH sebanyak 5 mL
Pada daerah Q perubahan pH dari 4 ke 6 dengan penambahan volume NaOH sebanyak 18 mL
Pada daerah R perubahan pH dari 7 ke 10 terjadi saat volume NaOH sebanyak 25 mL
Larutan penyangga tersebut akan menyangga pada pH asam karena dibentuk dari asam lemah dan basa kuat. Jadi daerah yang pH > 7 bukan daerah larutan penyangga. Jadi kemungkinan daerah larutan penyangga yaitu P atau Q. Dengan penambahan volume yang lebih banyak dan perubahan pH nya sedikit maka Q merupakan daerah larutan penyangga
JAWABAN A
(1) etilen glikol dapat ditambahkan ke dalam radiator mobil; Dan
(2) desalinasi air laut
Kedua contoh diatas berhubungan dengan sifat koligatif larutan secara berturut-turut…
- tekanan osmotic dan kenaikan titik didih
- kenaikan titik didih dan penurunan titik beku
- penurunan titik beku dan kenaikan titik didih
- penurunan tekanan uap dan tekanan osmotik
- penurunan titik beku dan osmosis balik
PEMBAHASAN :
(1) etilen glikol ditambahkan ke dalam radioator mobil berfungsi untuk menurunkan titik beku air jika dalam cuaca bersalju
(2) desalinasi air laut merupakan aplikasi dari tekanan osmosis. Dengan diberikan tekanan akan terjadi peristiwa reversibel osmosis (osmosis balik)
JAWABAN E
(1)NH3(aq) dan NH4Cl(aq)
(2)HCN(aq) dan NaCN(aq)
(3)H2PO4(aq)dan HPO42-(aq)
(4)CH3COOH(aq) dan CH3COONa(aq)
(5)H2CO3(aq) dan HCO3–(aq)
Komponen larutan penyanga yang terdapat cairan luar sel makhluk hidup adalah..
- 1
- 2
- 3
- 4
- 5
PEMBAHASAN :
Yang merupakan komponen larutan penyanga yang terdapat cairan luar sel makhluk hidup yaitu H2CO3(aq) dan HCO3–(aq), sedangkan komponen larutan penyanga yang terdapat diluar cairan luar sel makhluk hidup yaitu H2PO4(aq)dan HPO42-(aq)
JAWABAN E
1. bahan pembuat anilina;
2. pengawet kayu;
3. bahan pembuat semir sepatu;
4. pengawet makanan ;dan
5. bahan baku pembuatan peledak
Kegunaan dari nitrobenzena adalah…
- (3) dan (4)
- (3) dan (5)
- (1) dan (3)
- (1) dan (2)
- (4) dan (5)
PEMBAHASAN :
1. bahan pembuat anilina yaitu nitro benzena
2. pengawet kayu kegunaan dari fenol
3. bahan pembuat semir sepatu kegunaan dari nitrobenzen
4. pengawet makanan kegunaan dari asam benzoat
5. bahan baku pembuatan peledak kegunaan dari anilin dan toluena
JAWABAN C
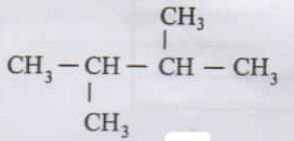
PEMBAHASAN :
Titik didih alkana akan tergantung pada rangka dari alkana, dalam jumlah c yang sama rantai lurus memiliki titik didih yang lebih tinggi dibanding rantai bercabang. Jika jumlah C nya berbeda maka alkana dengan rantai c panjang memiliki titik didih yang lebih besar dibanding rantai alkana yang pendek
JAWABAN C
- Galaktosa : Tidak terbentuk warna merah-ungu saat uji molisch
- Laktosa : Diperoleh dari hidrolisis amilum dengan bantuan enzim
- Glukosa : Hasil tes fehling menghasilkan warna ungu
- Sukrosa : Tidak menghasilkan Cu2O dengan pereaksi fehling
- Amilum : Tidak terjadi perubahan warna saat bereaksi dengan iodin
PEMBAHASAN :
(1) Galaktosa : Tidak terbentuk warna merah-ungu saat uji molisch (semua karbohidrat akan menghasilkan warna merah-ungu saat uji molisch)
(2) Laktosa : Diperoleh dari hidrolisis amilum dengan bantuan enzim (hidrolisis amilum menghasilkan glukosa)
(3) Glukosa : Hasil tes fehling menghasilkan warna ungu (tes fehling seharusnya menghasilkan endapan merah bata)
(4) Sukrosa : Tidak menghasilkan Cu2O dengan pereaksi fehling (benar)
(5) Amilum : Tidak terjadi perubahan warna saat bereaksi dengan iodin (seharusnya iodin menghasilkan warna biru jika diberi iodin)
JAWABAN D
(1) proses reaksi cepat
(2) didalam ditemukan sebagai garam mineral
(3) tidak stabil terhadap pemanasan
(4) gas hasil pembakarannya dapat mengeruhkan air kapur
(5) relatif lebih stabil terhadap pemanasan
Karakteristik yang dimiliki senyawa organik adalah..
- (1) dan (2)
- (2) dan (3)
- (2) dan (4)
- (3) dan (4)
- (4) dan (5)
PEMBAHASAN :
Karakteristik senyawa organik
(1) proses reaksi lambat
(2) Umumnya non elektrolit
(3) tidak stabil terhadap pemanasan
(4) gas hasil pembakarannya dapat mengeruhkan air kapur
(5) kurang stabil terhadap pemanasan
(6) Titik didih dan titik cair rendah
(7) Berikatan kovalen
(8) Lebih mudah larut dalam pelarut non polar
(9) Apabila dibakar menghasilkan karbon, CO2, dan H2O
JAWABAN D
- -CHO
- -CHO-
- -O-
- -OH
- -COOH
PEMBAHASAN :
– Alkohol primer jika dioksidasi akan menghasilkan aldehid, jika dioksidasi lanjut akan menghasilkan asam karboksilat
– Alkohol sekunder jika dioksidasi akan menghasilkan keton
– Alkohol tersier tidak dapat dioksidasi
JAWABAN B

Pasangan yang tepat dari senyawa karbon dan kegunaannya adalah…
- 1 dan 2
- 1 dan 3
- 3 dan 4
- 2 dan 3
- 4 dan 5
PEMBAHASAN :
Kegunaan beberapa senyawa organik diantaranya:
Formalin : pengawet
Dietil eter : obat bius, pelarut
Aseton : pelarut
Gliserol : bahan peledak membentuk nitrogliserin
Etanol 70% : antiseptik
JAWABAN E
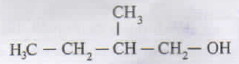
Nama IUPAC salah satu isomer dari senyawa tersebut adalah
- 2-metil-1-butanol
- 2-metil butanal
- 2-metil-2-butanol
- asam butanoat
- 2-butanon
PEMBAHASAN :
Pada gambar senyawa tersebut termasuk senyawa alkohol dengan jumlah atom C sebanyak 5 buah. Dapat berisomer gugus fungsi dengan eter, namun karena di pilihan tidak ada senyawa eter. Maka isomer senyawa bisa alkohol dengan jumlah atom C yang sama tapi dengan rangka atau posisi yang berbeda.
JAWABAN C
CH3-CH=CH2 + HCl → X
Rumus stuktur senyawa X yang terbentuk adalah..
PEMBAHASAN :
Menurut Markovnikoff, H dari HCl akan masuk ke C diantara ikatan rangkap yang jumlah H nya lebih banyak. sehingga hasil reaksinya
CH3-CH=CH2 + HCl → CH3-CHCl-CH3 + H2
JAWABAN D
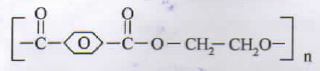
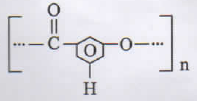
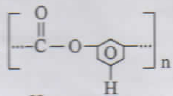
Nama polimer dan kegunaanya adalah..
- dakron, serat sintetis
- nilon 66, karpet
- protein, pembentuk jaingan tubuh
- bakelit, alat-alat listrik
- orlon, kaos kaki
PEMBAHASAN :
Nama polimer dengan struktur tersebut adalah dakron kegunaannya serat sintesis pengganti sutra alami
JAWABAN A
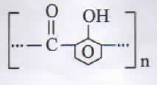
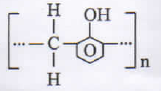
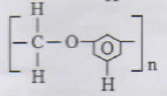
PEMBAHASAN :
polimer yang dapat dibentuk dari fenol dan formaldehid yaitu bakelit
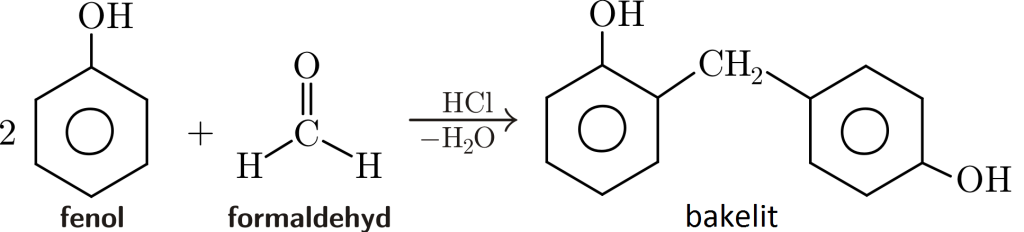
JAWABAN B
(1) sumber utama dari tubuh
(2) sebagai cadangan energi bagi tubuh
(3) pembentuk antibodi terhadap racun yang masuk dalam tubuh
(4) biokatalis pada proses metabolisme
(5) menyeimbangkan suhu tubuh
Pasangan yang merupakan kegunaan dari protein adalah….
- 1 dan 3
- 1 dan 2
- 3 dan 4
- 2 dan 5
- 3 dan 5
PEMBAHASAN :
fungsi dari protein:
(1) pembentuk antibodi terhadap racun yang masuk dalam tubuh
(2) biokatalis pada proses metabolisme
(3) alat angkut
(4) pengatur gerakan
(5) penyusun jaringan
(6) cadangan makanan
(7) pengatur reaksi
(8) pengendali pertumbuhan
JAWABAN C
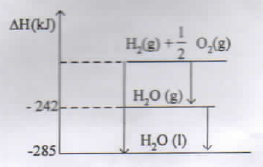
Pada penguapan 2 mol air dari tubuh diperlukan energi sebesar..
- 484
- 570
- 242
- 86
- 43
PEMBAHASAN :
reaksi penguapan air ditunjukan oleh panah merah
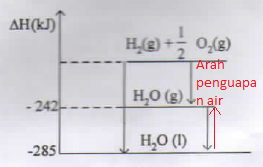
reaksi tersebut untuk penguapan 1 mol (koefisiennya = 1), untuk 1 mol ΔH nya adalah
ΔH = Hakhir – Hawal = -242 – (-285) = +43 kJ
Yang ditanyakan adalah untuk 2 mol, berarti:
ΔH = 2 x +43 kJ = +86 kJ
JAWABAN D
(1) C6H12O6 (aq) → 2C2H5OH (aq) + 2CO2 (g)
(2) C6H12O6 (aq) + O2 → 6CO2 (g) + 6H2O (l)
(3) H2O (aq) → H2(g) + 1/2 O2 (g)
(4) C8H18 (g) + 12 1/2 O2 (g) → 8CO2 (g) + 9H2O (g)
(5) C(s) + 2H2O (g) → CO2 (g) + 2H2(g)
Reaksi eksoterm terjadi pada…
- 1 dan 5
- 1 dan 3
- 2 dan 4
- 2 dan 5
- 3 dan 5
PEMBAHASAN :
Contoh reaksi eksoterm yang lain adalah:
- Reaksi pembakaran
- Reaksi netralisasi asam dan basa
- Reaksi korosi/pengkaratan
- Reaksi polimerisasi
- Respirasi
- Dekomposisi tumbuhan menjadi kompos
reaksi yang termasuk reaksi eksoterm adalah no 2 dan 4. Reaksi 2 adalah reaksi respirasi sedangkan reaksi 4 adalah reaksi pembakaran
JAWABAN C
CO (g) + 2H2 (g) ⇔ CH3OH (g)
Harga tetapan kesetimbangan Kc adalah…
- 1,50.10-1
- 1,67.10-3
- 66,67
- 600
- 6,67
PEMBAHASAN :

JAWABAN D
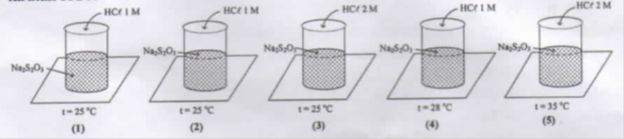
Laju reaksi yang hanya dipengaruhi oleh suhu terdapat pada gambar…
- 1 dan 4
- 2 dan 3
- 2 dan 5
- 3 dan 4
- 4 dan 5
PEMBAHASAN :
Untuk menentukan pengaruh suhu, lihat dua gelas kimia yang suhunya berbeda tapi konsentrasi HClnya sama. 2 gelas kimia tersebut adalah 1 dan 4. Pada gelas kimia 1 suhunya 25oC dengan HCl 1 M dan untuk gelas kimia 4 suhunya 28oC dengan konsentrasi HCl yang sama yaitu 1 M.
JAWABAN A
N2O4 (g) ⇔ 2NO2 (g) ΔH = -Q kJ
Jika volume ruangan diperbesar kesetimbangan akan bergeser ke arah..
- kanan karena jumlah mol hasil reaksi lebih besar
- kiri karena proses reaksi eksoterm
- kiri karena proses reaksi endoterm
- kanan karena jumlah mol pereaksi lebih kecil
- kanan karena proses reaksi eksoterm
PEMBAHASAN :
Asas Le Chatelier jika volume diperbesar maka akan menggeser reaksi ke jumlah koefisien yang lebih besar (wujud gas), jumlah koefisien ruas kiri = q, sedangkan jumlah koefisien ruas kanan = 2. Maka jika volume diperbesar reaksi akan bergeser ke kanan karena koef/mol nya lebih besar.
JAWABAN A
Mg(s) + 2 HCl(aq) → MgCl2(aq)+ H2

Laju reaksi pembentukan gas H2 adalah….
- 0,02 ml.det-1
- 0,15 ml.det-1
- 0,50 ml.det-1
- 0,05 ml.det-1
- 0,10 ml.det-1
PEMBAHASAN :
Ambil dua percobaan, kita ambil percobaan 1 dan 2
![]()
JAWABAN C
- 20 jam
- 124 jam
- 333 menit
- 19.989 menit
- 33,3 menit
PEMBAHASAN :
menentukan mol F2 (STP)
n = V/22,4 L = 23,2/22,4L = 1,036 mol
menentukan mol e dari perbandingan koefisien dengan mol F2
![]()
menentukan waktu dari mol e
![]()
![]()
JAWABAN C
Mn2+ + 2e– → Mn Eo= – 1,20 volt
In3+ + 3e– → In Eo= – 0,34 volt
Zn2++ 2e– → Zn Eo= – 0,76 volt
Ag+ + e– → Ag Eo= + 0.80 volt
Notasi sel yang berlangsung tidak spontan adalah…
- Mn/Mn2+//Zn2+/Zn
- Zn/Zn2+//Ag+/Ag
- Mn/Mn2+//Ag+/Ag
- Zn/Zn2+//In3+/In
- In/In3+//Mn3+/Mn
PEMBAHASAN :
Reaksi yang berlangsung spontan adalah reaksi yang berlangsung dengan sendirinya ditandai dengan Eonya bernilai +, sedangkan Reaksi yang berlangsung tidak spontan adalah reaksi yang tidak berlangsung dengan sendirinya ditandai dengan Eonya bernilai –
A. Mn/Mn2+//Ag+/Ag Eo = 0,8 – (-1,2) v = + 2,0 volt (spontan)
B. Zn/Zn2+//Ag+/Ag Eo = 0,8 – (-0,76) v = + 1,56 volt (spontan)
C. Mn/Mn2+//Zn2+/Zn Eo = (-0,76)-(-1,2) v = + 0,44 volt (spontan)
D. Zn/Zn2+//In3+/In Eo = (-0,34)-(-0,76) v = + 0,42 volt (spontan)
E. In/In3+//Mn3+/Mn Eo = (-1,20)-(-0,34) v = – 0,86 volt (tidak spontan)
JAWABAN E
CO(g) + H2O(g) ⇔ CO2(g) + H2(g)
Jika saat setimbang, perbandingan konsentrasi zat-zat bereaksi sebagai berikut:
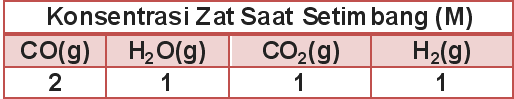
Harga tetapan kesetimbangan reaksi tersebut adalah…
- 1/2
- 4
- 1
- 8
- 2
- dilapisi dengan alumunium
- dilapisi oleh perak
- proteksi katodik
- dilumuri dengan oli
- dilapisi dengan seng
PEMBAHASAN :
Cara pencegahan dari korosi:
- pengecatan
- dilumuri dengan oli
- proteksi katodik
- pelapisan
Karena akan melindungi hiasan rumah maka cara untuk melindungi dari korosi yaitu dilapisi dengan logam perak. Perak akan sulit berkarat karena sukar mengalami oksidasi. Perak juga memiliki nilai keindahan untuk hiasan rumah
JAWABAN B
2Ca3(PO4)2(s) + 6SiO2(s) + 10C(s) → 6CaSiO3(s) + 10C(g) + P4(g)
Reaksi ini dilakukan pada suhu 1500 oC ,dipanaskan dengan kokas dan pasir. Nama proses pembuatan unsur tersebut adalah…
- goldschmidt
- deacon
- frasch
- wohler
- down
PEMBAHASAN :
Reaksi tersebut merupakan proses pembuatan posfor yang dikenal dengan nama prosesnya yaitu wohler
goldschmidt = pengolahan krom
deacon = pengolahan klorin
frasch = pengolahan belerang/sulfur
down = pengolahan Natrium
JAWABAN D
- PbSO4
- CaSO4
- MgSO4
- K2SO4
- Cr2(SO4)3
PEMBAHASAN :
Sifat-sifat diatas merupakan sifat yang dimiliki oleh logam transisi, sifat-sifat tersebut yaitu:
1. Logam
2. Titik didih tinggi
3. Bersifat paramagnetik
4. Memiliki beberapa bilangan oksidasi
5. Dapat menjadi katalis reaksi
6. Dapat membentuk ion kompleks
7. Ionnya berwarna
Yang termasuk logam transisi yaitu : Sc, Ti, V, Cr, Mn, Fe, Co, Ni, Cu, Zn
JAWABAN E
(1) memancarkan radiasi partikel alpha
(2) reaksinya menyebabkan perubahan inti
(3) bilangan okidasinya bervariasi
(4) menghantarkan arus listrik
Sifat unsur radioaktif adalah…
- 3 dan 4
- 1 dan 2
- 2 dan 4
- 1 dan 3
- 2 dan 3
PEMBAHASAN :
Sifat-sifat radioaktif:
1. Intinya tidak stabil
2. memancarkan radiasi partikel alpha, beta dan gamma
3. mengalami reaksi inti yang menyebabkan perubahan inti
JAWABAN B
(1) NaOH
(2) NaHCO3
(3) KCl
(4) Mg(OH)2
(5) CaSO4.2H2O
(6) CaCO3
Senyawa yang dapat digunakan untuk membuat sabun dan menetralkan asam lambung adalah…
- 1 dan 2
- 1 dan 4
- 4 dan 5
- 2 dan 3
- 5 dan 6
PEMBAHASAN :
Golongan IA yang digunakan untuk sabun yaitu NaOH, sedangkan golongan IIA yang digunakan sebagai obat maag yaitu Mg(OH)2
JAWABAN B