Halo selamat datang di semester 2. Bab pertama kimia semester 2 untuk kelas 10 adalah larutan elektrolit dan non elektrolit. Larutan itu tidak semuanya dapat menghantarkan listrik yah ada juga yang tidak bisa menghantarkan listrik. Simak rangkuman materi dan contoh soal larutan elektrolit dan non elektrolit untuk kamu kelas 10, jika ingin lebih paham kita buatkan juga video pembelajarannya disini. Selamat belajar
DAFTAR ISI
Rangkuman Materi Larutan Elektrolit dan Non Elektrolit Kelas 10
Berdasarkan daya hantar listrik, maka larutan dibagi menjadi dua bagian:
Larutan Elektrolit
Larutan elektrolit merupakan larutan yang dapat menghantarkan listrik. Berdasarkan kuat lemahnya larutan elektrolit dibedakan menjadi dua:
Larutan elektrolit kuat
Larutan ini sangat baik dalam menghantarkan listrik. Dalam percobaan uji daya hantar listrik, larutan elektrolit kuat akan menyalakan lampu dengan terang dan menghasilkan gelembung yang banyak. Ciri-ciri dari larutan elektrolit kuat adalah:
- Mengalami ionisasi sempurna, artinya zat elektrolit akan terionisasi keseluruhannya. Hal ini disebabkan karena mengalami reaksi searah atau berkesudahan.
HCl(aq) → H+(aq) + Cl-(aq) - Memiliki Derajat Ionisasi (α) = 1, α merupakan perbandingan antara mol yang terionisasi dengan mol mula-mula. Karena semua mol mula-mula terionisasi maka perbandingannya akan bernilai = 1
- Contohnya : Asam kuat (HCl, HBr, HI, H2SO4, HNO3, HClO4, HClO3), Basa kuat (LiOH, NaOH, KOH, RbOH, CsOH, Ca(OH)2, Sr(OH)2, Ba(OH)2, dan sebagian garam.
Larutan elektrolit lemah
Larutan ini kurang baik dalam menghantarkan listrik. Dalam percobaan uji daya hantar listrik, larutan elektrolit lemah akan menyalakan lampu dengan redup bahkan mati tetapi menghasilkan gelembung walaupun sedikit. Ciri-ciri dari larutan elektrolit lemah adalah:
- Mengalami ionisasi sebagian, artinya zat elektrolit akan terionisasi sebagiannya saja. Hal ini disebabkan karena mengalami reaksi kesetimbangan.
HCN(aq) → H+(aq) + CN-(aq) - Memiliki Derajat Ionisasi (α) = 0 < α < 1, α merupakan perbandingan antara mol yang terionisasi dengan mol mula-mula. Karena sebagian mol mula-mula terionisasi maka perbandingannya akan bernilai diantara 0 sampai 1
- Contohnya : Asam lemah (CH3COOH, H3PO4, HCN, HF, dll), Basa lemah (AgOH, Zn(OH)2, NH4OH, dll).
Larutan Non elektrolit
Larutan elektrolit merupakan larutan yang tidak dapat menghantarkan listrik. Ciri-ciri dari larutan non elektrolit adalah:
- Tidak mengalami ionisasi artinya zat non elektrolit hanya terjadi perubahan wujudnya saja tidak berubah menjadi ion.
C6H12O6(s) → C6H12O6(aq) - Memiliki Derajat Ionisasi (α) = 0. Karena mol mula-mula tidak ada yang terionisasi maka perbandingannya akan bernilai diantara 0
- Contohnya : Gula (glukosa C6H12O6, sukrosa C12H22O11), Urea (CO(NH2)2), Alkohol (metanol (CH3OH), etanol (C2H5OH))
Video Pembelajaran Larutan Elektrolit & Non Elektrolit Larutan Kelas X
Videonya ada 2 part ya. Kalau terlalu kecil tekan opsi full screen di pojok kanan video. Silahkan menyimak!
- Part 1
- Part 2
Contoh Soal Larutan Elektrolit dan Non Elektrolit & Pembahasannya Kelas 10
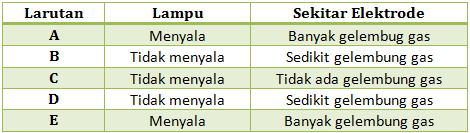
PEMBAHASAN :
Termasuk larutan elektrolit : Larutan A, E (Lampu menyala dan banyak gelembung), B dan D ( ada sedikit gelembung)
Elektrolit Kuat : Larutan A, E (Lampu menyala dan banyak gelembung)
Elektrolit Lemah : B dan D (ada sedikit gelembung)
Larutan non elektrolit : Larutan C (Tidak menyala dan tidak ada gelembung gas)
PEMBAHASAN :
K2SO4 → 2K+ + SO42-
HNO3 → H+ + NO3-
Fe2(SO4)3 → 2Fe3+ + 3SO42-
Ba(NO3)2 → Ba2+ + 2NO3-
PEMBAHASAN :
Larutan elektrolit merupakan larutan yang dapat menghantarkan listrik sedangkan larutan non elektrolit larutan yang tidak dapat menghantarkan listrik. Larutan elektrolit dapat menghantarkan listrik karena dalam larutannya terdapat ion-ion yang dapat melepaskan elektron dan menangkap elektron sehingga elektron dapat mengalir diantara dua kutub.
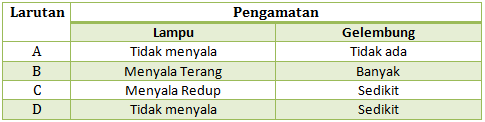
PEMBAHASAN :
Hasil daya hantar listrik beberapa larutan dalam uji daya hantar listrik:
- Larutan elektrolit kuat : lampu menyala terang, gelembung banyak.
- Larutan elektrolit lemah : lampu menyala redup/tidak menyala, gelembung sedikit.
- Larutan non elektrolit : lampu tidak menyala, gelembung tidak ada.
Dari ciri-ciri di atas, maka
- Larutan A : larutan non elektrolit
- Larutan B : larutan elektrolit kuat
- Larutan C : larutan elektrolit lemah
- Larutan D : larutan elektrolit lemah
PEMBAHASAN :
- larutan BaSO4 merupakan garam yang termasuk ke dalam larutan elektrolit kuat
- Larutan AgOH merupakan basa lemah yang termasuk kedalam elektrolit lemah
- Larutan C12H22O11 (sukrosa/gula putih) merupakan larutan non elektrolit
Berdasarkan ciri-ciri larutan elektrolit dan non elektrolit pada soal no 2, maka:
- Larutan BaSO4 lampu menyala terang, gelembung banyak.
- Larutan AgOH lampu menyala redup, gelembung sedikit
- Larutan C12H22O11 lampu mati, tidak ada gelembung.
Tuliskan reaksi ionisasi dari larutan berikut:
a.Ca(NO3)2
b.Zn(OH)2
c.CO(NH2)2
PEMBAHASAN :
a. Ca(NO3)2 → Ca2+ + 2NO3-
b. Zn(OH)2 → Zn2+ + 2OH-
c. CO(NH2)2 → CO(NH2)2 (tidak mengalami ionisasi)
- HBr 0,1 M
- H2SO4 0,1 M
- NH3 0,1 M
- C2H5OH
PEMBAHASAN :
HBr dan H2SO4 merupakan larutan elektrolit kuat, NH3 merupakan larutan elektrolit lemah sedangkan C2H5OH merupakan larutan non elektrolit. HBr dan H2SO4 keduanya merupakan elektrolit kuat dengan molaritas yang sama. H2SO4 lebih kuat elektrolitnya karena mengandung ion yang lebih banyak.
H2SO4 → 2H+ + SO42- (3 ion)
HBr → H+ + Br- (2 ion)
PEMBAHASAN :
Garam dapur (NaCl) merupakan senyawa ion yang termasuk larutan elektrolit kuat. Senyawa ion jika dalam bentuk padat belum memiliki ion-ion yang bergerak bebas. Sedangkan dalam bentuk cair dan larutannnya NaCl sudah memiliki ion-ion yang dapat menghantarkan listrik
- aseton
- alkohol
- larutan NaCl
- larutan urea
- larutan cuka
- larutan gula
- air laut
PEMBAHASAN :
Yang termasuk larutan elektrolit:
- air laut (elektrolit kuat)
- larutan cuka (elektrolit lemah)
- larutan NaCl (elektrolit kuat)
Yang termasuk larutan non elektrolit
- larutan gula
- larutan urea
- aseton
- alkohol
PEMBAHASAN :
Larutan Elektrolit kuat:
- larutan garam (NaCl)
- air laut
- Larutan H2SO4
- Larutan HBr
- Larutan HCl
- Larutan HI
- Larutan HNO3
- Larutan KI
- Larutan BaCl2
- Larutan HClO4
Larutan Elektrolit lemah:
- Larutan cuka (CH3COOH)
- Larutan HCN
- Larutan amoniak (NH4OH)
- Larutan AgOH
- Larutan HF
- Larutan H2S
- Larutan Fe(OH)3
- Larutan Zn(OH)2
- Larutan Al(OH)3
- Larutan HNO2
Larutan Non Elektrolit
- Larutan gula (C12H22O11)
- Larutan Urea (CO(NH2)2)
- Larutan Aseton (C3H6O)
- Etanol (C2H5OH)
- Metanol (CH3OH)
- Larutan glukosa (C6H12O6)
- Larutan Fruktosa
- Propanol (C3H7OH)
- Butanol (C4H9OH)
- n-heksana
PEMBAHASAN :
elektrolit dibagi menjadi dua yaitu elektrolit kuat dan elektrolit lemah. Elektrolit kuat dan lemah dibedakan berdasarkan jumlah ion yang dihasilkan ketika mengalami reaksi ionisasi. Perbedaan jumlah ion pada jumlah yang sama (konsentrasi sama) menyebabkan perbedaan daya hantar listriknya berbeda. Pada konsentrasi yang sama elektrolit kuat dapat menyalakan lampu dengan terang dan menghasilkan gelembung yang banyak sedangkan elektrolit lemah menyalakan lampu hingga redup atau bisa saja mati tapi menghasilkan gelembung walaupun sedikit.
- HCl 1 M atau HCl 2 M
- HCl 1 M atau CH3COOH 1 M
- HCl 1 M atau H2SO4 1 M
PEMBAHASAN :
- HCl 1 M atau HCl 2 M
Untuk zat yang sama, maka kekuatan daya hantar listrik dilihat dari besarnya konsentrasi atau molaritas. Semakin besar konsentrasi semakin banyak ionnnya sehingga semakin kuat menghantarkan listrisnya. Maka HCl 2 M larutan yang menghantarkan listriknya lebih baik. - HCl 1 M atau CH3COOH 1 M
Pada konsentrasi sama maka HCl merupakan larutan yang menghantarkan listrisnya lebih baik. Larutan HCl merupakan larutan elektrolit kuat yang jika terionisasi akan terionisasi sempurna sedangkan larutan CH3COOH termasuk larutan elektrolit lemah jika terionisasi maka akan mengalami terionisasi sebagian. - HCl 1 M atau H2SO4 1 M
Larutan HCl dan H2SO4 keduanya merupakan larutan elektrolit kuat namun kekuatan elektrolit juga dipengaruhi oleh jumlah ion. Semakin banyak jumlah ion semakin kuat larutan elektrolitnya. HCl memiliki 2 ion yaitu H+ dan Cl- sedangkan H2SO4 memiliki 3 ion yaitu 2H+ dan SO42- , sehingga pada konsentrasi yang sama H2SO4 memiliki sifat elektrolit yang lebih kuat dibanding HCl.
PEMBAHASAN :
Kristal NaCl sudah memiliki ion-ion di dalamnya namun tidak dapat bergerak bebas. Sedangkan jika dilarutkan ke dalam air ion-ion NaCl dapat bergerak bebas dan dapat mengalirkan elektron sehingga dapat menghantarkan listrik.
Soal Pilihan Ganda
- partikel yang bergerak bebas
- molekul-molekul yang bergerak bebas
- kemampuan larut dalam air
- atom-atom yang bergerak bebas
- ion-ion yang bergerak bebas
PEMBAHASAN :
Suatu larutan dapat menghantarkan listrik jika di dalamnya terdapat ion-ion yang bergerak bebas. Ion-ion ini ada yang melepaskan elektron dan menerima elektron sehingga terjadi pergerakan elektron antara dua kutub yang akan terus mengalirkan listrik. Pada larutan non elektrolit tidak terdapat ion-ion bebas sehingga elektron akan terhenti di salah satu kutub.
- Larutan A elektrolit lemah, larutan B elektrolit kuat
- Larutan A elektrolit kuat, larutan B elektrolit lemah
- Larutan A non elektrolit, larutan B elektrolit kuat
- Larutan A elektrolit lemah, larutan B non elektrolit
- Larutan A non elektrolit, larutan B elektrolit lemah
PEMBAHASAN :
Larutan A lampu pada alat uji mati tetapi menghasilkan gelembung walaupun sedikit dapat disimpulkan termasuk larutan elektrolit lemah, elektrolit lemah dapat menyebabkan lampu menyala redup atau mati tetapi menghasilkan gelembung udara di elektroda. Larutan B termasuk elektrolit kuat karena menyebabkan lampu pada alat uji menyala terang dan menghasilkan gelembung udara yang banyak.
Jawaban A
- NaCl dan HBr
- NaCl dan KBr
- HBr dan HCl
- gula dan urea
- H2SO4 dan KCl
PEMBAHASAN :
Zat yang dalam keadaan padat tidak menghantar dan pada keadaan cair dan larutan mengantar listrik adalah senyawa ion. Senyawa ion tersusun dari unsur logam dan logam. Yang termasuk senyawa ion adalah NaCl dan KBr. Sedangkan HBr, H2SO4, HCl, termasuk kedalam senyawa kovalen polar yang dapat menghantar listrik pada keadaan larutan. sedangkan gula dan urea termasuk kovalen non polar sehingga tidak dapat menghantar pada wujud apapun
Jawaban B
- H2SO4 (aq) → 2H+ (aq) + 4SO2- (aq)
- H2SO4 (aq) → H2+ (aq) + 4SO2- (aq)
- H2SO4 (aq) → 2H+ (aq) + SO42- (aq)
- H2SO4 (aq) → H2+ (aq) + SO42- (aq)
- H2SO4 (aq) →H2+ (aq) +4SO2- (aq)
PEMBAHASAN :
Reaksi ionisasi larutan H2SO4 adalah
H2SO4 (aq) → 2H+ (aq) + SO42- (aq)
Jawaban C
- K2SO4
- AgCl
- HCl
- CO(NH2)2
- HCN
PEMBAHASAN :
- K2SO4 → 2K+ + SO42-, Jumlah ionnya ada 3 ion
- AgCl → Ag+ + Cl-, Jumlah ionnya ada 2 ion
- HBr → H+ + Br- , Jumlah ionnya ada 2 ion
- CO(NH2)2, tidak mengalami ionisasi
- HCN ⇔ H+ + CN- , Jumlah ionnya ada 2 ion
Jawaban A
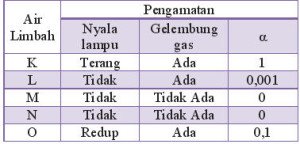
Pasangan air limbah yang bersifat elektrolit kuat dan non elektrolit adalah…
- K dan M
- K dan L
- L dan M
- L dan O
- L dan N
PEMBAHASAN :
Ciri elektrolit kuat:
– Nyala lampu terang
– Gelembung banyak
– derajat ionisasi (α) =1
Ciri elektrolit lemah:
– nyala lampu redup/mati
– gelembung sedikit
– derajat ionisasi 0<α<1
Ciri non elektrolit:
– nyala lampu mati
– tidak ada gelembung
– α = 0
Jawaban A
- larutan non elektrolit
- larutan elektrolit
- larutan garam
- larutan asam
- larutan basa
PEMBAHASAN :
Larutan yang dapat menghantarkan listrik disebut larutan elektrolit. Larutan elektrolit dibagi menjadi dua jenis yaitu:
- larutan elektrolit kuat, menghantarkan listrik dengan baik ditandai dengan lampu yang menyala terang dan menghasilkan banyak gelembung.
- larutan elektrolit lemah, menghantarkan listrik kurang baik ditandai dengan lampu yang menyala redup atau mati dan menghasilkan sedikit gelembung.
Jawaban B
- larutan C12H22O11 2,0 M
- larutan NaBr 2,0 M
- larutan CO(NH2)2 2,0 M
- larutan K2SO4 2,0 M
- larutan AgOH 2,0 M
PEMBAHASAN :
Kekuatan menghantar listrik yang paling baik dimiliki oleh larutan elektrolit kuat dengan jumlah ion yang lebih banyak.
- larutan C12H22O11 (sukrosa) 2,0 M, termasuk larutan non elektrolit
- larutan NaBr 2,0 M, termasuk larutan elektrolit kuat dengan jumlah ion 2
NaBr → Na+ + Br- - larutan CO(NH2)2 (urea) 2,0 M, termasuk larutan non elektrolit
- larutan K2SO4 2,0 M, termasuk larutan elektrolit kuat dengan jumlah ion 3
K2SO4 → 2K+ + SO42- - larutan AgOH 2,0 M, termasuk elektrolit lemah
Maka pada konsentrasi yang sama larutan yang menghantarkan paling baik adalah K2SO4 2,0 M
Jawaban D
- HCl
- C2H5OH
- CaBr2
- HF
- CO(NH2)2
PEMBAHASAN :
Berikut penjelasan masing-masing opsi:
- HCl, termasuk larutan elektrolit dari senyawa kovalen karena terdiri dari non logam dan non logam.
- C2H5OH, termasuk larutan non elektrolit.
- CaBr2, termasuk larutan elektrolit dari senyawa ion karena terdiri dari logam dan non logam.
- HF, termasuk larutan elektrolit dari senyawa kovalen karena terdiri dari non logam dan non logam.
- CO(NH2)2, termasuk larutan non elektrolit.
Maka Jawaban yang tepat adalah C
Jawaban C
- nyala lampu mati
- menghasilkan sedikit gelembung udara
- Larutan asam cuka
- Larutan gula
- Larutan urea
- Larutan asam klorida
- Larutan kalium hidroksida
PEMBAHASAN :
Dari data percobaan maka larutan yang dimaksud adalah larutan elektrolit lemah. Penjelasan tiap opsi yaitu:
- Larutan asam cuka (CH3COOH) merupakan larutan elektrolit lemah.
- Larutan gula (C12H22O11) merupakan larutan non elektrolit
- Larutan urea (CO(NH2)2) merupakan larutan non elektrolit
- Larutan asam klorida (HCl) merupakan larutan elektrolit kuat
- Larutan kalium hidroksida (KOH) merupakan larutan elektrolit kuat
Maka Jawaban yang tepat adalah A
Jawaban A
- atom-atom unsur penyusunnya bergerak bebas dalam air
- ion unsur penyusunnya dapat bergerak bebas dalam air
- larut dalam air tanpa menghasilkan ion-ionnya.
- menguraikan air menjadi ion H+ dan OH-
- menghasilkan sedikit gelembung.
PEMBAHASAN :
Suatu larutan non elektrolit tidak menghantarkan listrik karena ketika dilarutkan ke dalam air tidak menghasilkan ion-ionnya atau tetap menjadi molekkul-molekulnya, sehingga tidak ada aliran listrik yang terjadi akibat serah terima elektron
Jawaban C
Gimana belajar larutan elektrolit & non elektrolitnya, kalau ada yang kurang paham bisa kamu tanya di kolom komentar yah. Ok demikian rangkuman materi dan contoh soal larutan elekrolit dan non elektrolit berikut video pembelajarannya. Semoga berguna buat kalian. Kalau bermanfaat bantu kita juga yah untuk share dan beritahu teman kamu untuk berkunjung kesini. Terima kasih.
Sumber Soal : Kelas X Penerbit Erlangga Pengarang Unggul Sudarmo
Fitur Terbaru!!
Kini kamu bisa bertanya soal yang tidak ada di artikel kami.
Ajukan pernyataan dan dapatkan jawaban dari tim ahli kami.
Untuk bertanya KLIK DISINI


Makasih ilmunya kak, bermanfaat… Kak, itu nomer 17 bukannya harusnya optionnya C ya kak…
Sama2. makasih koreksinya
hai kak admin,thank u so much yaa kak sudah membuat latihan soal yang bener-bener bermanfaat buat saya yang mau PTS kimia 🙂